
◎注射用曲拉西利是先声药业与G1 Therapeutics合作的创新药,值得注意的是,注射用曲拉西利也是全球首个且唯一具有全面骨髓保护功效的药物,可以有效降低化疗引起的骨髓抑制的发生率。
◎曲拉西利获批稍迟,但其将首个申报上市的适应症转移到骨髓保护,与同靶点产品具有差异化的布局,成为CDK4/6抑制剂在骨髓保护领域的First-in-class。
◎从全球研发进度来看,CD112R属于一款尚待挖掘的靶点。药渡数据显示,截至12月9日,仅有Compugen以及Surface Oncology两家的临床试验获批。值得注意的是,这两家的CD112R产品均吸引到了国际药企巨头的注意。
每经记者|许立波 每经编辑|魏官红

《掘金创新药》由每日经济新闻联合药渡数据共同推出,旨在解读新药研发进展与趋势,剖析产品竞争力与市场前景,洞察医药资本脉络,见证医药产业高质量发展。

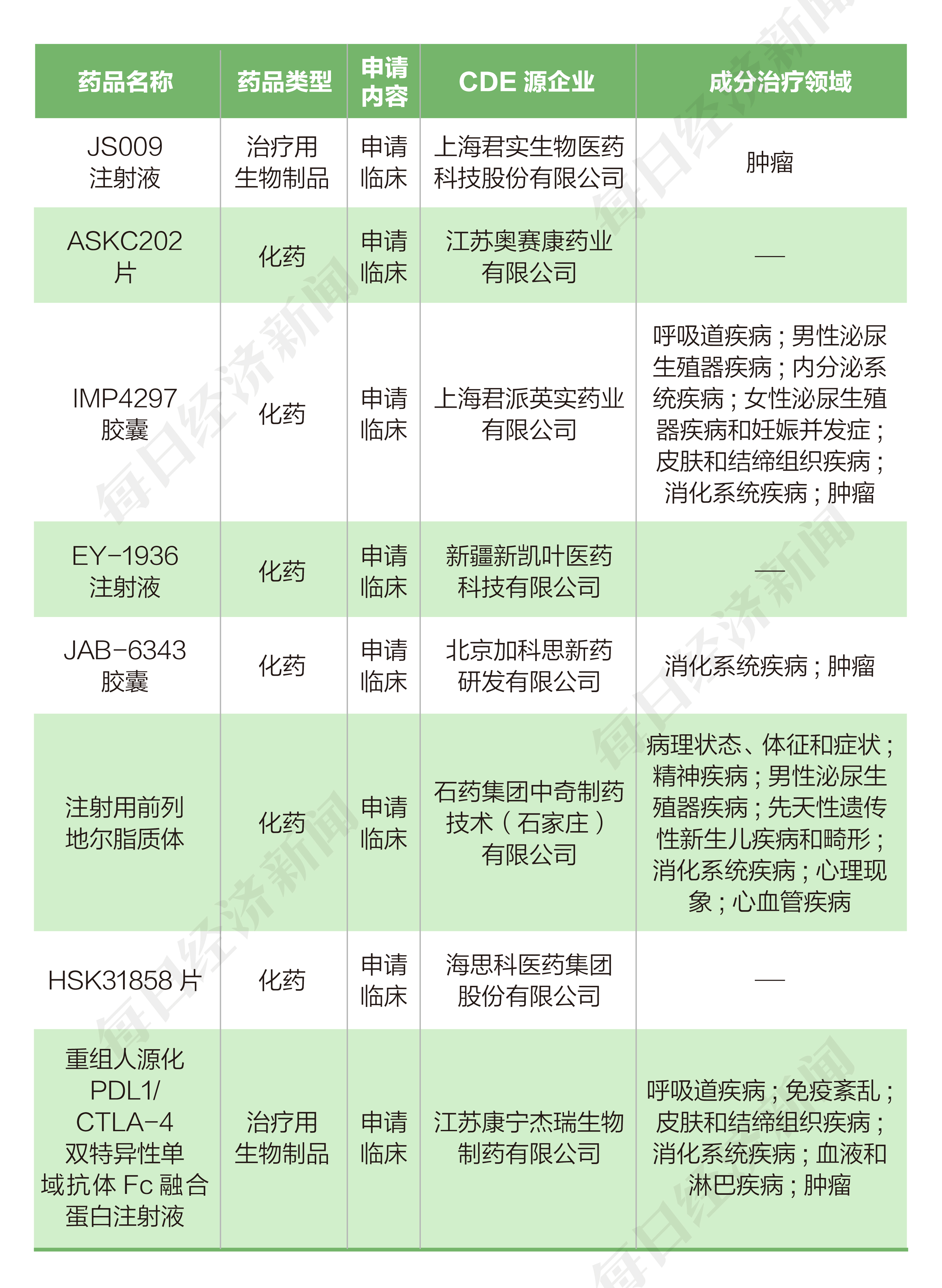
根据药渡数据,11月29日至12月3日,国家药品监督管理局药品审评中心(CDE)共收到7家上市公司提交的8个化学新药、治疗用生物制品新药申请。

本周上市公司方面,君实生物-U(688180.SH)申报2个临床申请,康宁杰瑞制药-B(09966.HK)、奥赛康(002755.SZ)、复星医药(600196.SH)、加科思-B(01167.HK)、石药集团(01093.HK)、海思科(002653.SZ)各申报1个临床申请。
1、先声药业递交注射用曲拉西利新药上市申请 系首个骨髓保护CDK4/6抑制剂
2021年11月29日,先声药业(02096.HK)公告称,中国国家药品监督管理局(NMPA)已受理注射用曲拉西利(英文通用名Trilaciclib)的境外生产药品注册上市许可申请,拟在接受含铂类药物联合依托泊苷方案的广泛期小细胞肺癌(ES-SCLC)患者中预防性使用。12月8日,CDE官网显示,先声药业注射用曲拉西利的上市申请(受理号:JXHS2101087)按“符合附条件批准的药品”拟纳入优先审评审批程序。
注射用曲拉西利是先声药业与G1 Therapeutics合作的创新药,2020年8月,先声药业与G1公司达成独家授权合约,以总计1.7亿美元的金额获得曲拉西利在大中华地区所有适应症的开发和商业化权益。今年2月,G1公司的Trilaciclib已在美国获得FDA批准上市。值得注意的是,注射用曲拉西利也是全球首个且唯一具有全面骨髓保护功效的药物,可以有效降低化疗引起的骨髓抑制(CIM)的发生率。
根据药渡数据,自2020年8月先声药业引进这款产品之后,次年1月用于治疗实体瘤的I期临床试验开展;迄今已经获批3项临床试验申请。从研发进展看,针对小细胞肺癌、三阴性乳腺肿瘤、结直肠癌、转移性乳腺癌等适应症均已进入III期临床阶段。
行业洞察:全球共有4款CDK4/6抑制剂上市 辉瑞的Ibrance占据优势份额
根据2020年世界卫生组织国际癌症研究机构(IARC)发布的数据,乳腺癌已成为全球第一大恶性肿瘤,是女性最常见的恶性肿瘤之一。而在国内,乳腺癌也已经位列女性肿瘤发病谱首位,乳腺癌发病率占全身各种恶性肿瘤发病率的9.1%;乳腺癌患者死亡病例约11.72万例。其中,HER2(人表皮生长因子受体2)阳性乳腺癌约占全部乳腺癌的20%~25%,
通过靶向细胞周期机制,中断刺激恶性细胞增殖的细胞内及促有丝分裂激素信号,CDK4/6抑制剂或能有效治疗乳腺癌。目前,CDK4/6抑制剂已被国家综合癌症网络列入HR+/HER2-mBC的一线治疗药物。
据国盛证券测算,在目前全球范围内上市的4款CDK4/6抑制剂中,辉瑞的Ibrance占据优势份额,2021年上半年销售收入26.57亿美元,G1的Trilaciclib由于上市时间较晚,目前尚无具体数据。

图片来源:国盛证券研报截图
而在国内市场,辉瑞的Ibrance、礼来的Verzenio均已获批上市,诺华的Kisqali也已于10月底在国内递交上市申请。
从国内企业在CDK4/6抑制剂上的研发进度来看,药渡数据库显示,进展最快的是恒瑞的达尔西利(Dalpiciclib),已于今年4月申报上市;山东轩竹的吡罗西尼(Birociclib)紧随其后,已经进入III期临床;其余国内厂商则尚处于II期或I期临床阶段。
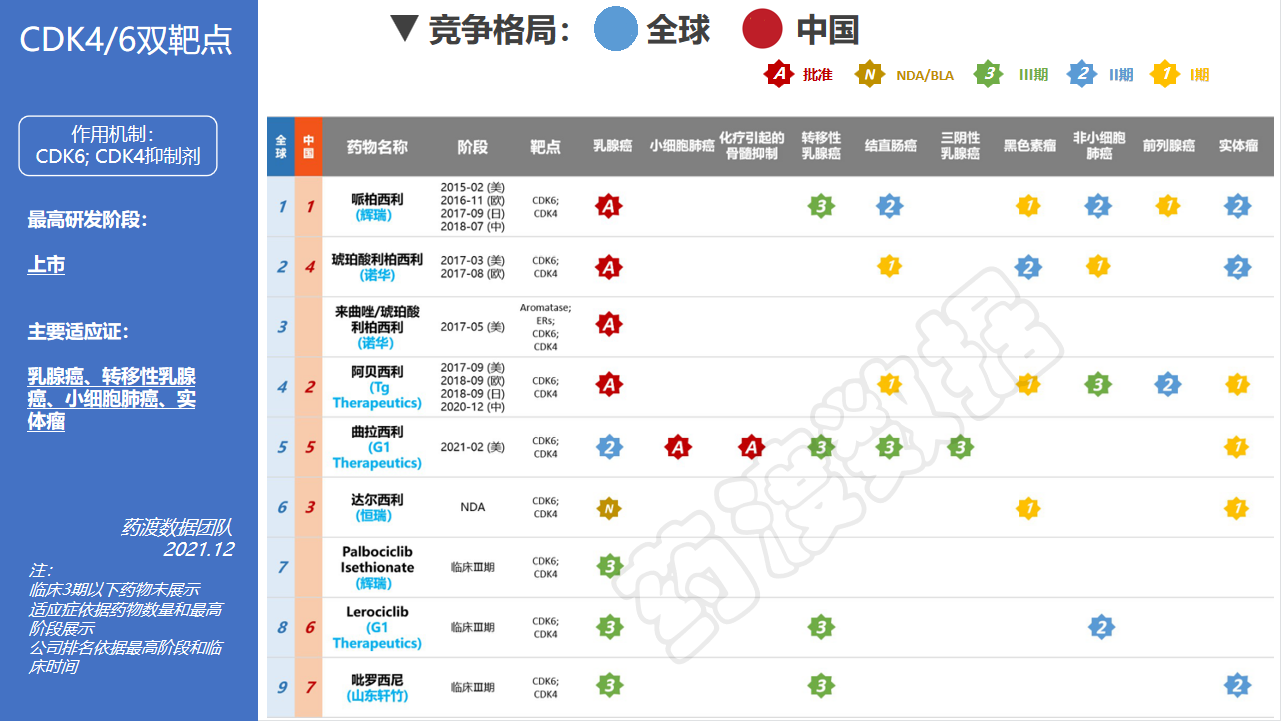
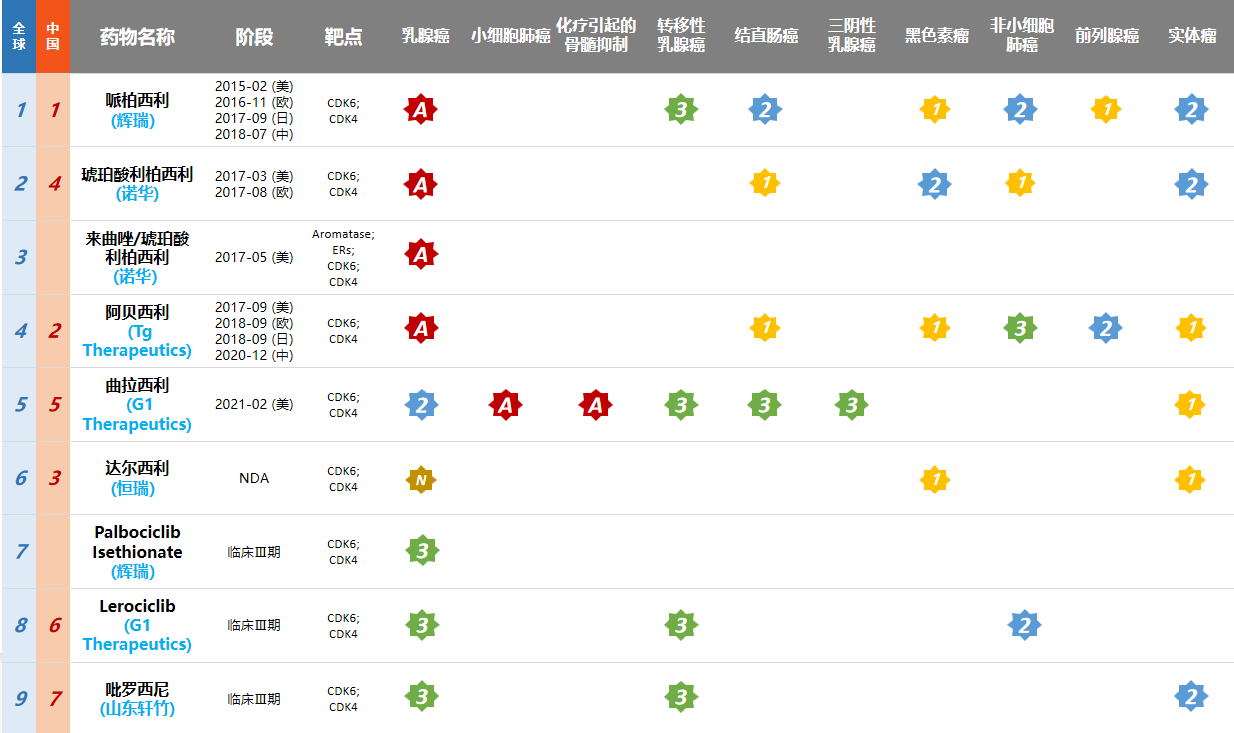
点评:
从市场销售看,最先获批的辉瑞Ibrance市场表现强势,2020年全球销售额达到53.92亿美元且仍在增长。巨大市场潜力下后继者不断,从市场份额来看,诺华和礼来两家增速可观,正在加速拓展自己的CDK4/6版图,辉瑞的先发优势并不稳妥。
在CDK4/6抑制剂的红海竞争中,曲拉西利获批稍迟,但其将首个申报上市的适应症转移到骨髓保护,与同靶点产品具有差异化的布局,避开了与其他三款CDK4/6抑制剂的直接竞争,成为CDK4/6抑制剂在骨髓保护领域的First-in-class。
2、君实生物CD112R单抗申报临床 License-out前景广阔
12月3日,君实生物公告称,收到国家药品监督管理局核准签发的《受理通知书》,JS009注射液的临床试验申请获得受理。JS009是君实生物独立自主研发的重组人源化抗CD112R单克隆抗体注射液,主要用于晚期恶性肿瘤的治疗。JS009也是国内首个获得药物临床试验申请受理的抗CD112R单克隆抗体。目前,国内外尚无同类靶点产品获批上市。
根据君实生物公告,CD112R又名PVRIG(脊髓灰质炎病毒受体相关免疫球蛋白结构域),是PVR家族的一个单跨膜蛋白,主要表达于T细胞和NK细胞上,并在细胞激活后有明显的表达上调。CD112R与抗原递呈细胞和部分肿瘤细胞表面的CD112具有高亲和力,结合后可抑制T细胞和NK细胞的抗肿瘤作用。JS009能以高亲和力特异性地结合CD112R,有效阻断CD112R与其配体CD112信号通路,进而促进T细胞和NK细胞的活化和增殖,增强免疫系统杀伤肿瘤细胞的能力。同时JS009选择了IgG4亚型,可降低抗体依赖的细胞介导的细胞毒性作用(ADCC)和补体依赖的细胞毒性(CDC)。
此外,TIGIT是PVR家族的另一个免疫抑制靶点,其配体有PVR和CD112,且其结合CD112的位点不同于CD112R。临床前体内药效实验显示,JS009与公司自主研发的特异性抗TIGIT单克隆抗体注射液(项目代号“JS006”)联合治疗,表现出显著的协同抗肿瘤作用。
行业洞察:仅有两款CD112R药物获批临床 已引起药企巨头注意
从全球研发进度来看,CD112R属于一款尚待挖掘的靶点。药渡数据显示,截至12月9日,仅有Compugen以及Surface Oncology两家的临床试验获批,其中Compugen的COM-701进展稍快,已进入临床II期;Surface Oncology的SRF-813,其IND申请则刚刚在12月1日获得美国FDA的批准。
值得注意的是,Compugen以及Surface Oncology两家的CD112R产品均吸引到了国际药企巨头的注意,前者与BMS达成了一笔价值1200万美元的股权投资合作,同时BMS也将旗下的Opdivo(PD-1单抗)免费提供,以进行COM701联合Opdivo用于治疗晚期实体癌的临床试验合作;后者则与GSK达成了一项授权合作协议,根据协议条款,GSK将支付8500万美元的预付款,此外,Surface Oncology还有可能获得最多7.3亿美元的里程金以及销售收入。
点评:
《掘金创新药》研究员认为,JS004是全球首个进入临床的抗BTLA单抗,目前君实生物在创新前沿靶点的布局丰富,在全球范围内还拥有CD112R,CD39,CD93等First-in-Class的靶点管线,参照上述两家公司在CD112R上的授权收益,License-out前景广阔。
正如中泰证券在研报中的评价,君实生物生产和商业化能力不断加强,在明年能够看到较明显的基本面拐点。
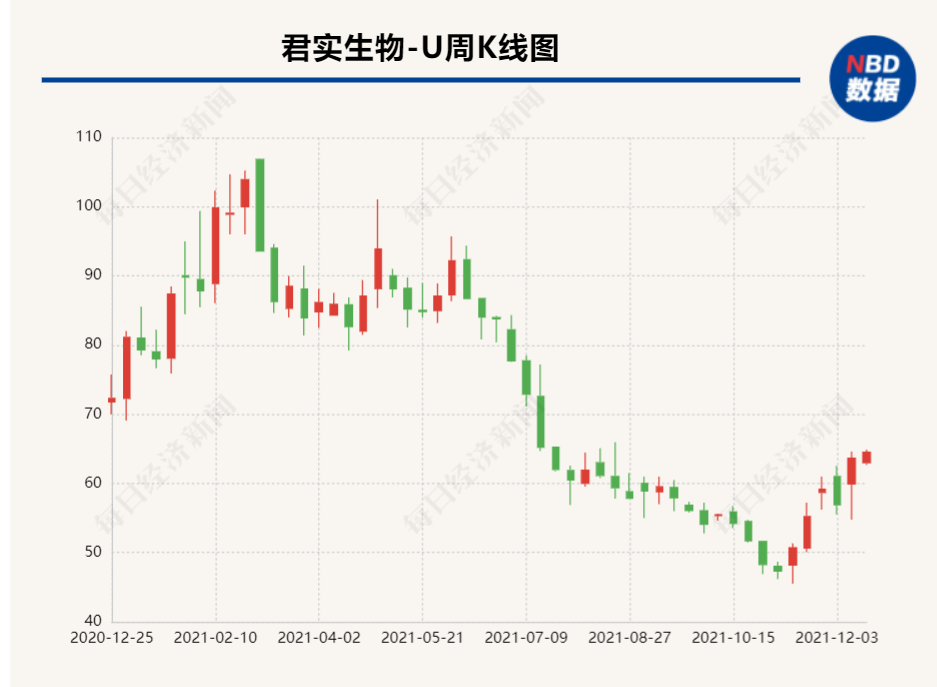
而在股价方面,此前受PD-1激烈竞争的影响,自今年6月以来,君实生物股价相较于年内高点106.98元/股已跌去近一半,但这样的走势在最近似乎有所改观。一方面,虽然PD-1在价格和市场方面仍面临巨大的竞争压力,但资本市场已逐渐消化;另一方面,市场也对PD-1之外的创新药,尤其是部分原研首创或是同类最佳的产品抱有更多期待。
封面图片来源:摄图网-500205422

1本文为《每日经济新闻》原创作品。
2 未经《每日经济新闻》授权,不得以任何方式加以使用,包括但不限于转载、摘编、复制或建立镜像等,违者必究。
