
◎目前,“以患者为中心”的药物研发理念已渐成共识。Clare Grace介绍,研究结果显示,以患者为中心的策略能够显著优化临床试验的流程和结果,其中使用以患者为中心的试验研发的药物的上市概率为87%,远高于传统试验68%的比例;此外,在受试者招募时间缩短40%的基础上,招募率也能够提升50%。
每经记者|许立波 每经编辑|文多

图片来源:视觉中国
近年来,随着政策的鼓励支持与药企研发策略的不断调整,“以患者为中心”的药物研发理念已渐成共识。尤其是去年8月以来,我国药品监管部门密集出台一系列文件,国家药监局药品审评中心(CDE)连续就3项以患者为中心的临床试验相关指导原则征求意见,标志着我国药物研发“以患者为中心”时代的开启。
近日,精鼎医药首席患者官Clare Grace在接受包括每日经济新闻在内多家媒体采访时表示,根据精鼎医药联手经济学人智库发布的报告,一项纳入4000个具备以患者为中心要素的临床试验、20000个传统试验的研究展现出的结果显示,以患者为中心的策略能够显著优化临床试验的流程和结果,其中使用以患者为中心的试验研发的药物的上市概率为87%,远高于传统试验68%的比例;此外,在受试者招募时间缩短40%的基础上,招募率也能够提升50%。
“但问题在于,每一位患者的需求都是不一样的,这意味着设计临床试验时要为患者提供各式各样的、灵活的选择,以使患者尽可能方便地参与并进行更为广泛的研究。”Clare Grace表示。
2022年8月,国家药品监督管理局药品审评中心(CDE)就《以患者为中心的临床试验获益-风险评估技术指导原则(征求意见稿)》、《以患者为中心的临床试验设计技术指导原则(征求意见稿)》、《以患者为中心的临床试验实施技术指导原则(征求意见稿)》征求意见。上述征求意见稿中提到,以患者需求为出发点、视患者为主动参与者、以临床价值为最终目的的药物研发理念。
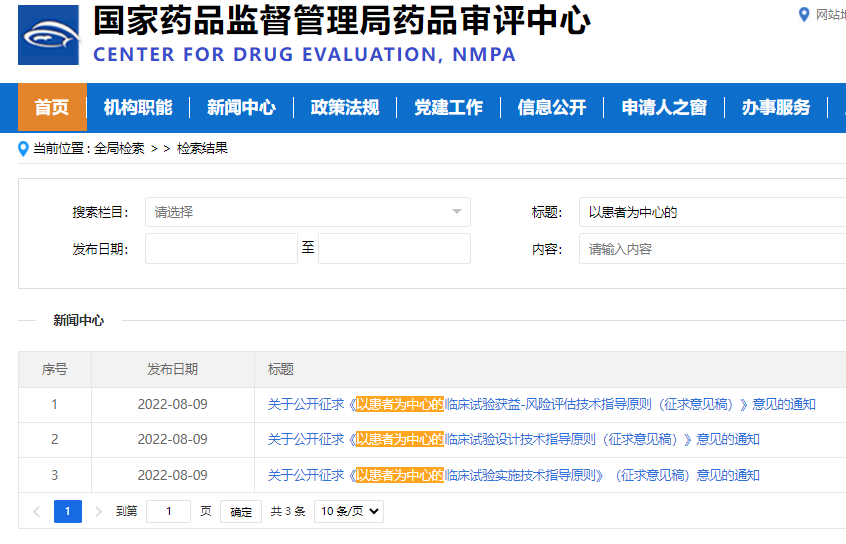
图片来源:国家药品监督管理局药品审评中心网站截图
2022年11月,CDE又发布了《组织患者参与药物研发的一般考虑指导原则(试行)》,鼓励患者参与到药物研发的全生命周期中。试行指导原则主要是便于申请人通过良好的组织患者参与药物研发工作,更好地获得患者的体验信息和数据,提高整体药物研发的质量和成功率,惠及患者、改善临床用药现状,增加临床用药的选择。
CDE在文件中表示,作为药物临床试验的受试者和医疗实践的对象,患者对疾病状态和治疗有亲身体会,可为药物研发提供更贴近患者期望、更有价值的信息。因此,“以患者为中心”的理念已经逐步从患者用药端延伸至药品研发端,患者身份也从过去的被动接受治疗转变为主动参与制定研发,鼓励患者参与药物研发全周期被越来越多的药企接受。
Clare Grace透露,目前精鼎医药在研项目或者已经上市的项目中,已经有80%的临床试验在设计和执行上应用了“以患者为中心”元素。而在政策指引之下,除了精鼎医药,未来也会有更多药品申办方会计划采用“以患者为中心”的临床试验。
值得注意的是,《组织患者参与药物研发的一般考虑指导原则(试行)》还将患者的范畴进行了拓展,与一般意义上临床试验中的受试者概念所不同,上述《指导原则》中的患者不仅为患者个体,还包括患者的家属、监护者、看护者以及患者组织等,即“患者个体”还可以在不参加任何药物临床试验的情况下提供意见。
对此,Clare Grace回应《每日经济新闻》记者称,从精鼎医药的角度来说,公司也在内部设置了患者顾问委员会并邀请来自全球不同地区的患者参与到顾问委员会;这些委员会不仅仅有患者参与其中,其中也纳入了一些患者的看护人、照料者和家属,这些患者的利益相关方对于支持患者、了解患者需求发挥了重要的作用。
“在与患者倡导组织合作过程中,我们发现这些正式的患者倡导组织能够进一步汇集有关患者需求的重要信息并提示长期的趋势。此外,有时候患者并不知道如何为他们自己发声,他们可能缺乏涉及到药物研发和临床试验的专业知识,所以通常需要患者倡导组织从中发挥作用,在我们和患者之间搭建一座桥梁。”Clare Grace表示。

图片来源:视觉中国
临床试验未来最大的变化之一是向远程智能临床试验(DCT)的转变。
公开资料显示,远程智能临床试验是通过远程医疗和移动/当地医疗资源执行的临床试验流程,是一种以患者为中心的分散式模式。
精鼎医药高级副总裁、亚太区企业战略负责人兼中国区负责人郑唯玲表示,目前在国内可执行度最高的两个远程智能临床试验元素,一个是eCOA/ePRO(electronic Clinical Outcome Assessment/electronic Patient Reported Outcome,即用电子化的方式搜集临床结局评估数据/患者报告主观/体验数据),另一个是Tele Visit(远程访视,即临床研究人员可以通过视频/语音,在临床研究期间与受试者进行远程随访)。
Clare Grace则表示,在远程智能临床试验解决方案中有非常多的关注点,每个考量因素都是非常不一样的,适用于不同的疾病阶段。如可穿戴设备和传感器特别适用于心血管疾病,检查心律、关注患者在行走过程中有没有震颤等,可穿戴设备和传感器可以看到并实时观察特定患者的状态。在患者无法来到医院进行数据监测的情况下,通过这种方式可以获得更高质量的参数和数据,让医生能够更好地了解患者的状态。

图片来源:视觉中国
对于其他的临床研究来说,比如在肿瘤领域,家庭护理的重要性则更为凸显,其可以让患者,特别是行动受限的患者减少出行时间,足不出户就能获得医疗服务,也让患者更有意愿参与到临床研究中。
此外,远程智能临床试验也有助于增加受试者的多样性,来自不同背景和地点的人可以参与,所有这些因素都加快了药物开发过程。
不过,Clare Grace也表示,当前远程智能临床试验面临着监管上的挑战。特别是在数据安全和隐私方面,随着越来越多的个人信息被数字化收集和存储,一旦这些数据未被妥善保护,其泄露所造成的后果可能会非常严重。此外,在不同的国家和区域,对于医疗支付和报销也有一些非常严格的监管要求,比如要求医院要对远程医疗进行报销,抑或是关于远程智能临床试验其他方面的报销,这也是监管者所关注的内容。
“另外,我也相信大多数DCT能够确保使用同样的流程,以进一步推进临床研究的开展。例如上门护理中,我们需要向监管部门证明,随访人员和研究中心的护士、医生接受着相同的培训,因为监管部门所寻求的重大变化是要能够确保提供有效的监督。研究中心的运营是非常容易的,因为医生毕竟就在医院,他们能够在现场直接督导研究团队如何展开临床研究。而相较之下,如果融入了远程元素,则需要PI(Principle investigator,临床研究项目负责人)来监督,以确保远程研究的人员能够有效执行,或是能够定期在系统中进行校验、确保数据完整。关于这方面的监督,相较于普通的临床研究,DCT文件的归档记录有所不同,需要有更广泛的归档记录。”Clare Grace表示。
封面图片来源:视觉中国

1本文为《每日经济新闻》原创作品。
2 未经《每日经济新闻》授权,不得以任何方式加以使用,包括但不限于转载、摘编、复制或建立镜像等,违者必究。
