
◎按照卡度尼利单抗的定价方案和患者救助方案,年治疗费用不高于19.8万元。但较派安普利单抗有利的是,卡度尼利单抗能“踩点”赶上今年的医保谈判。《掘金创新药》研究员认为,未来卡度尼利单抗若能顺利通过谈判被纳入医保目录,将有望通过医保加速进院速度,从而实现产品的加速放量。
◎OT-401是首款且唯一可以持续稳定在眼内释放氟轻松,用于治疗眼部慢性非感染性葡萄膜炎的first in class药物,其获批填补了国内葡萄膜炎治疗领域的空白。因此,在国内市场上,OT-401尚属无竞品格局。
每经记者|陈星 每经编辑|魏官红

《掘金创新药》由每日经济新闻联合药渡数据共同推出,旨在解读新药研发进展与趋势,剖析产品竞争力与市场前景,洞察医药资本脉络,见证医药产业高质量发展。

根据药渡数据,2022年6月20日至2022年7月1日,国家药品监督管理局药品审评中心(CDE)共收到17家上市公司(含上市公司控股公司或上市公司披露研发进展的主体公司)提交的20个化学新药、预防用生物制品、治疗用生物制品新药申请。

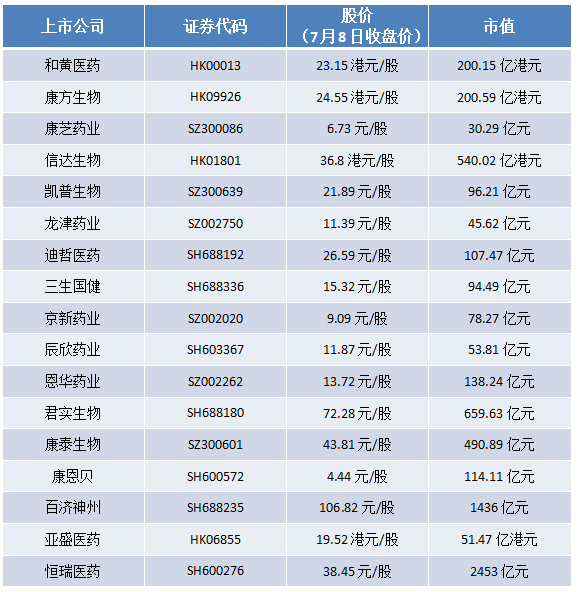
2022年6月20日至7月1日期间,上市公司方面,和黄医药(00013.HK)、康芝药业(300086.SZ)、康方生物(09926.HK)、信达生物(01801.HK)、凯普生物(300639.SZ)、龙津药业(002750.SZ)、迪哲医药(688192.SH)、三生国健(688336.SH)、京新药业(002020.SZ)、辰欣药业(603367.SH)、恩华药业(002262.SZ)、君实生物(688180.SH)、康泰生物(300601.SZ)、康恩贝(600572.SH)分别提交1个临床申请。亚盛医药(06855.HK)提交2个临床申请,恒瑞医药(600276.SH)提交3个临床申请。百济神州(688235.SH)提交1个生产申请。

1.首款国产双抗获批上市 年均费用20万元的药物能否让康方生物“翻身”?
6月29日,康方生物卡度尼利单抗注射液(AK104,商品名开坦尼)通过优先审评审批程序附条件批准上市,适用于既往接受含铂化疗治疗失败的复发或转移性宫颈癌患者的治疗。卡度尼利是首个获批上市的国产双抗,也是全球首款PD-1/CTLA-4双抗。
卡度尼利单抗注射液是一种靶向PD-1和CTLA-4的双特异性抗体,可阻断PD-1和CTLA-4与其配体PD-L1/PD-L2和B7.1/B7.2的相互作用,从而阻断PD-1和CTLA-4信号通路的免疫抑制反应,促进肿瘤特异性的T细胞免疫活化,进而发挥抗肿瘤作用。
此次卡度尼利单抗的获批是基于一项在中国开展的II期关键性临床研究结果。该试验入组患者为既往接受含铂化疗治疗失败的复发或转移性宫颈癌患者。该研究的结果已于2022年美国妇科肿瘤学会(SGO)年会上发表。
目前卡度尼利单抗还正在开发包括非小细胞肺癌、肝癌、胃癌、宫颈癌、肾癌及鼻咽癌等多种恶性肿瘤,多种研究处于临床II期或III期阶段。其中,转移性食管癌和转移性胃癌进展相对较快。
行业洞察:
从国内宫颈癌治疗市场来看,宫颈癌是全球和我国最常见的妇科肿瘤之一,在女性恶性肿瘤中,其发病率仅次于乳腺癌。数据显示,2020年全球新发60.4万例,死亡34.2万例,对应我国新发10.9万例,死亡5.9万例。
在宫颈癌预防和治疗领域,此前普及程度较高的是宫颈癌疫苗,但对于复发或转移性宫颈癌患者而言,治疗的需求同样迫切。并且,相较早期宫颈癌,复发或转移性宫颈癌预后差,治疗有限。
按照2022年第一版《NCCN子宫颈癌临床实践指南》的建议,顺铂被认为是对于转移性子宫颈癌最有效的药物,对于持续性或复发转移性子宫颈癌患者,在一定先决条件下,首先推荐帕博丽珠单抗+顺铂(或卡铂)+紫杉醇±贝伐珠单抗(1级证据)。
对于无法接受手术或放疗的患者,顺铂、卡铂或紫杉醇都是合理的一线单药方案,其中顺铂是复发或转移性子宫颈癌最有效的化疗单药。同样对于子宫颈癌同期放化疗的患者,通常也首选顺铂单药,顺铂不耐受者再考虑用卡铂。指南对于子宫颈癌的二线治疗药物主要包括白蛋白紫杉醇、帕姆单抗、多西他赛、贝伐珠单抗等。
这意味着,卡度尼利单抗的主要竞争对手将是帕博丽珠单抗(K药)、贝伐珠单抗、纳武利尤单抗(O药)及众多生物类似药。前几大原研药对手在国内已经上市多年,还拓展了多个适应症。据相关数据,2022年一季度贝伐珠单抗的销售额达到20亿元人民币,帕博利珠单抗达到4亿元,纳武利尤单抗达到9千多万元。市场前景广阔的同时,卡杜尼利单抗也将单挑诸多“前辈”。
而除了面对与原研药的竞争,国内已经有众多贝伐珠单抗的生物类似药上市。2019年,齐鲁制药的安可达作为首仿获批上市,2020年销售额就达到18亿元。齐鲁制药之后,国内又有数个贝伐珠单抗生物类似药上市。
公司点评:
在卡度尼利单抗获批前后的6月27日、29日和30日,康方生物股价分别收跌2.55%、3.95%和5.14%;但随后在7月4日,康方的股价大涨14.75%。股价的起伏或能在一定程度上代表外界对于康方生物双抗药物获批的看法。

图片来源:Wind截图
作为康方生物成立以来的最大亮点或者说是外界的最大期待,卡度尼利单抗的获批对公司而言,是一个新的里程碑,也验证了自己的研发实力。但如前文所述,卡度尼利单抗获批后的市场表现,关系到康方生物从研发到商业化利润的闭环能否打通。
康方生物创始人、董事长夏瑜于2021年接受《掘金创新药》研究员采访时曾表示,卡度尼利单抗的商业化将由公司自己进行,并透露公司已经在组建自己的商业化团队。康方生物2021年年报显示,公司销售团队已经超过500人,计划将在2022年扩展至800人。
但康方生物此前并无独立运作新药商业化的经验。
2021年,其首个商业化产品PD-1派安普利单抗获批上市销售,康方生物采取的方式是联合正大天晴推动该款药物的商业化。产品上市4个月,派安普利单抗实现销售额约2.12亿元,在一众PD-1产品中表现尚可。但同期,康方生物的销售费用也不低——达到了1.79亿元。此外,由于上市时间较晚,派安普利单抗错过了去年的医保谈判机会。
卡度尼利单抗上市后,外界最为关注的首先是其定价问题。
7月初,卡度尼利单抗的价格出炉——13220元/125mg/瓶,每次用药为3瓶,每两周给药。按照该定价方案和患者救助方案,年治疗费用不高于19.8万元。但较派安普利单抗有利的是,根据今年医保谈判设置的药物获批时间,卡度尼利单抗能“踩点”赶上今年的医保谈判。
《掘金创新药》研究员认为,未来卡度尼利单抗若能顺利通过谈判被纳入医保目录,将有望通过医保加速进院速度,从而实现产品的加速放量。今年派安普利单抗和卡度尼利单抗是否将申报参加2022年医保目录调整、如何报价等问题还有待观察。
2.欧康维视治疗非感染性葡萄膜炎药物获批,填补国内空白
6月20日,NMPA官网显示,欧康维视OT-401(氟轻松玻璃体植入剂,YUTIQ)获CDE新药上市批准,用于治疗累及眼后段的慢性非感染性葡萄膜炎。这是中国药品注册史上第一个完全基于“真实世界研究数据”申报上市的新药。
OT-401(YUTIQ)由欧康维视于2018年11月从EyePoint Pharmaceuticals引入,是同类药品中首创的、非生物降解的微型缓释注射型玻璃体内植入剂。OT-401(YUTIQ)的活性成分——氟轻松丙酮酯,是一类人工合成的皮质类固醇,作为局部抗炎药已经被广泛使用达30年之久。门诊单次植入3年内,按照预设的控制速度持续释放共计0.18 mg活性成分。
OT-401(YUTIQ)于2018年10月18日被美国FDA首次批准,也是迄今为止唯一一款用于治疗葡萄膜炎的药物。2020年11月30日,OT-401于欧康维视在海南博鳌启动“真实世界研究”。当年12月,OT-401被正式纳入海南省药品监督管理局药械临床真实世界数据首批药品试点品种名单中。
从真实世界数据中期报告来看,OT-401的使用能够显著降低NIU-PS患者葡萄膜炎术后复发率,植入后视力逐步上升,系统性激素用药、眼局部激素注射制剂、眼局部激素眼药水用量明显下降。与传统治疗方法相比,OT-401组葡萄膜炎复发率低、视力提高幅度明显、激素使用量明显减小。
行业洞察:
葡萄膜炎是一种眼睛炎症,也是全世界范围内导致失明的主要原因之一。如果不进行治疗,失明将是这种疾病的自然病程。糖皮质激素和免疫抑制剂是治疗葡萄膜炎的传统药物,虽然能暂时阻止疾病发展,但长期使用具有明显的毒副作用。
而非感染性葡萄膜炎是一种慢性葡萄膜炎,可引起白内障、青光眼,玻璃体混浊,黄斑病变等多种并发症,每一次炎症发作都会对眼内组织造成不可逆的损伤,持续炎症甚至可导致永久性视力丧失,因此其也是中国第二大致盲性眼病。
根据弗若斯特沙利文报告,2022年国内的累及眼后段的慢性非感染性葡萄膜炎患病人数约有150万人,巅峰渗透率若能做到3%-5%,总的目标患者群体约为4.5万至7.5万人。
OT-401是首款且唯一可以持续稳定在眼内释放氟轻松,用于治疗眼部慢性非感染性葡萄膜炎的first in class药物,具有低剂量眼内给药和长达36个月的持续作用时间的特点,其获批填补了国内葡萄膜炎治疗领域的空白。因此,在国内市场上,OT-401尚属无竞品格局。
公司点评:
除了OT-401获批上市,截至目前,欧康维视已拥有眼前及眼后段20种药物资产,其中6款产品已进入III期临床试验。公司管线实现了对近视、干眼症及眼底疾病等方向的全覆盖。
2021年由于干眼症和青光眼产品销售收入的增长,公司收入从0.13亿元增长至0.56亿元,公司的经调整后净亏损从2020年的2.77亿元收窄至2021年的1.87亿元。宣布OT-401上市后,欧康维视股价有一波明显上涨。
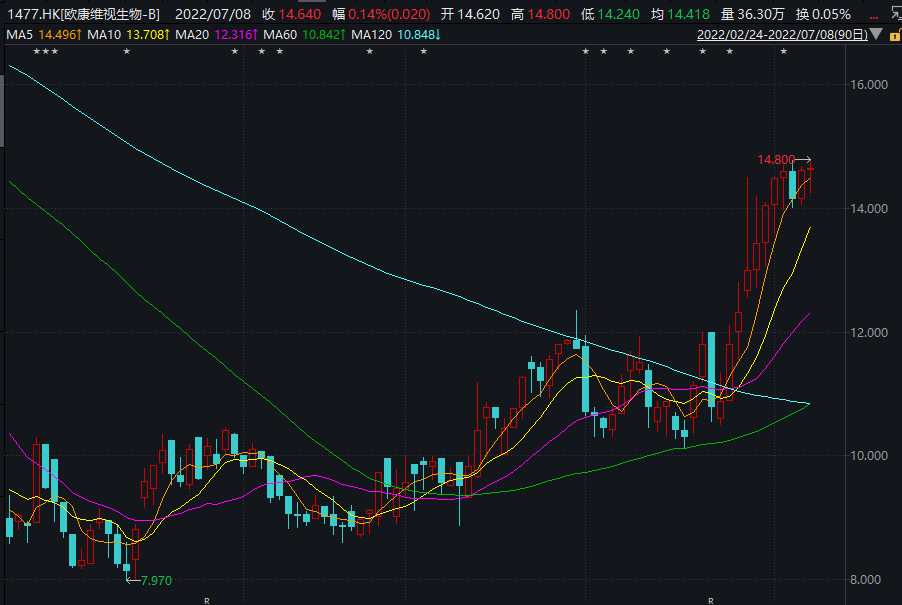
图片来源:Wind截图
在欧康维视的管线中,对青少年近视控制药物阿托品滴眼液亦有布局。与兴齐眼药(SZ300573,股价107.22元,94亿元)等其他研发企业不同的是,欧康维视OT-101的III期临床试验成为低浓度阿托品及其类似物全球首个包含中国人群在内的III期国际多中心临床试验(MRCT),商业化方向为在全球多国注册上市;二是OT-101去年10月在海南博鳌启动真实世界研究;三是OT-101使用独家设计的创新密闭式分体装置,解决低浓度阿托品溶液的稳定性问题。
目前,国内尚未有阿托品滴眼液正式获批上市。面对青少年近视这一广阔市场,众多企业虎视眈眈。
但《掘金创新药》研究员注意到,近期业内有传言称,相关部门已经开始整顿阿托品滴眼液在未获批情况下,提前通过互联网医院和院内制剂形式销售的现象。兴齐眼药等代表企业股价在多个交易日出现震荡下滑。若临床试验进展顺利,目前已经推进到临床III期的企业有望率先分得阿托品滴眼液的正规市场。
封面图片来源:摄图网-501514500

1本文为《每日经济新闻》原创作品。
2 未经《每日经济新闻》授权,不得以任何方式加以使用,包括但不限于转载、摘编、复制或建立镜像等,违者必究。
