
值得注意的是,虽然国内创新药企业势头猛烈,但未来可能要面临过度竞争的局面。过度竞争也就意味着要靠价格战拼市场,一些技术路线较为落后的产品可能会在产品迭代中被淘汰。
每经记者|金喆 每经编辑|魏官红

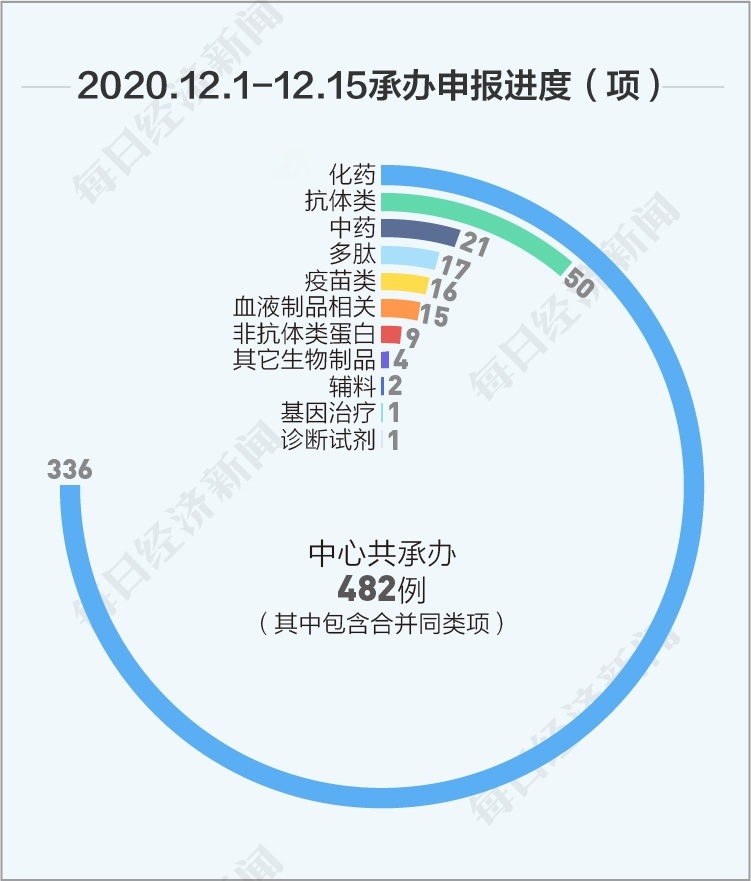
丁香园Insight数据库援引国家药品监督管理局药品审评中心数据显示,12月1日~12月15日,中心共承办482例申报进度。其中,受理化药申请336项,抗体类50项,中药申请21项,多肽17项,疫苗类16项,血液制品相关15项,非抗体类蛋白9项,其它生物制品4项,辅料2项,基因治疗1项,诊断试剂1项。
本阶段医药行业最大热点是2020年医保谈判,最热门品种自然绕不开PD-1。2019年,信达生物PD-1抗体药物降价近64%,全年费用降至约9.7万元,成为唯一进医保目录的PD-1。今年前三季度,信达生物PD-1销售额超过25亿元,由此可见医保的贡献作用。
根据丁香园Insight数据库,目前国内已有8个PD-1类产品上市,超过30种产品在研。今年的谈判,参与者更多、筹码也更多,最终哪家企业能进入医保后的大市场,值得外界关注。
但激烈、甚至称得上惨烈的价格竞争也给行业警示:虽然国内创新药企业势头猛烈,但因彼此扎堆的靶点和适应症差别不大,未来可能要面临过度竞争的局面。而过度竞争也就意味着又要靠价格战拼市场,一些技术路线较为落后的产品可能会在产品迭代中被淘汰。
1、2020年医保谈判结束,医药股普遍飘红
去年医保谈判时“灵魂砍价”的场景历历在目,今年12月17日靴子落地后,医药股集体暴涨。实际上,每年一次的医保谈判已逐渐常态化,企业也越来越适应这种节奏,只有降价是硬招数。
本轮医药板块强势反弹,与谈判降价效果比此前预估的要“温和”有关。此前,行业预期降价幅度将在80%以上,甚至达到90%。但根据目前流出的消息,降价幅度均没有此前预计的力度大,比如中成药降幅约40%,PD-1降价幅度约80%。
根据过往经验,进入医保目录对企业而言是利好,如果降价幅度低于预期的话,则是锦上添花。
兴业证券医药小组发布的研报指出,回顾过去创新药谈判,竞争格局较好的品种和竞争相对激烈的品种,在通过谈判纳入医保后,均能实现较快放量,给相应品种带来弹性空间。
“我们以曲妥珠单抗(生物类似物,尚未获批)和奥希替尼(竞品于今年刚上市)为例。从PDB样本医院数据来看,其在通过谈判纳入医保后均实现快速放量,极大地体现出纳入医保可以助推创新药加速放量增长。”兴业证券分析指出,纳入医保之前,虽然这些药物具备较高的临床价值,但因为价格相对较高而导致市场渗透率较低,进入医保之后这些药物的临床使用率得到迅速提升。
从企业角度来说,新药上市进入医保的周期缩短,如果顺利进入医保则意味着能快速放量,潜在患者规模和竞争格局的“量价”博弈还可以考虑。经过多轮国家医保谈判,企业对基本流程及需要准备的资料亦心中有数,现在医保调整周期基本明确,基本上一轮谈判结束,就要开始着手次年上市产品的准备工作。
但我们仍需要分析PD-1上市后的激烈竞争情况,为创新药下一步发展提供更明确的方向。
2018年6月,2款PD-1进口药获批,月费用约4万元,同年12月,2款国产药获批,月费用降到约1.4万元。2019年底医保谈判后,信达生物信迪利单抗医保后年费用约2.9万元。根据目前流出的消息,本次进入医保的国产PD-1患者实际支付的年治疗费用降至1.5万元左右。不过,《每日经济新闻》记者尚未从官方确认上述消息。
根据时间轴,药物上市后难以避免价格竞争,创新药研发难度大、资金需求高,如果扎堆在相同靶点,未来也可能跟PD-1的情况类似。广东省肺癌研究所名誉所长吴一龙等人总结了中国国内抗肿瘤药物的研发现状:截至2020年1月,中国有821种正在研究的抗肿瘤药物,其中包括404种me-too药物和359种first-in-class药物。
《每日经济新闻》记者根据数据统计,当前国内最新药物研发热门靶点包括PD-1/PD-L1、CTLA-4、CAR-T、CD20、EGFR、TNF-α等,大多集中在肿瘤治疗不同领域,并吸引了国内外企业的共同竞争。
2、恒瑞1类新药氟唑帕利胶囊即将获批,为首个国产
丁香园Insight数据库显示,12月3日,恒瑞医药1类新药「氟唑帕利胶囊」上市申请进入行政审批阶段,预计将在近日获批,该药是国内企业自主研发的首个PARP抑制剂,用于治疗既往经过二线及以上化疗的伴有BRCA1/2致病性或疑似致病性突变的复发性卵巢癌患者。
目前,全球共有4个PARP抑制剂上市。其中,奥拉帕利2018年在国内获批上市,并在2019年医保谈判中降价61.8%进入医保乙类目录,医保支付标准为169.00元(150mg/片),尼拉帕利2019年在国内获批上市。据Insight数据库,奥拉帕利全球销售额连年增长,在2019年已达到16.42亿美元,同比增长94.8%,市场潜力巨大。
恒瑞已针对氟唑帕利开展了26项临床,适应症涉及小细胞肺癌、实体瘤、复发转移三阴乳腺癌、前列腺癌、复发性卵巢癌、晚期胃癌等。其中,15项临床尚在进行中,包括4项III期临床。另外,国内已有多个企业布局PARP抑制剂,10个企业已进入临床阶段。
3、诺诚健华BTK抑制剂奥布替尼片即将获批上市
丁香园Insight数据库显示,近日,诺诚健华(09969,HK)奥布替尼片(orelabrutinib)在国内的注册申请进入“在审批”阶段,有望于近期获得批准,用于单药治疗既往至少接受过一种治疗的慢性淋巴细胞白血病/小淋巴细胞淋巴瘤(CLL/SLL)以及既往至少接受过一种治疗的套细胞淋巴瘤(MCL)。
这意味着奥布替尼将成为继伊布替尼、泽布替尼后,国内第三个获批上市的BTK抑制剂。
根据诺诚健华早前发布的临床研究数据,奥布替尼治疗复发难治性CLL/SLL患者的2期研究中,患者的总体客观缓解率(ORR)高达88.8%。在2020年美国血液学会(ASH)年会上,诺诚健华公布的2期研究更新数据显示:奥布替尼单药治疗复发/难治CLL/SLL中国患者,具有较高的完全缓解率(CR)、持久的反应和改善的安全性。
此外,诺诚健华还在探索奥布替尼治疗复发难治性边缘区淋巴瘤(MZL)、中枢神经系统白血病(CNSL)、华氏巨球蛋白血症(WM)、滤泡性淋巴瘤(FL)、多发性硬化(MS)等适应症的治疗效果。这意味着,未来奥布替尼有望惠及更多的患者。
1、本期首次注册上市的品种有10个(如下图所示)
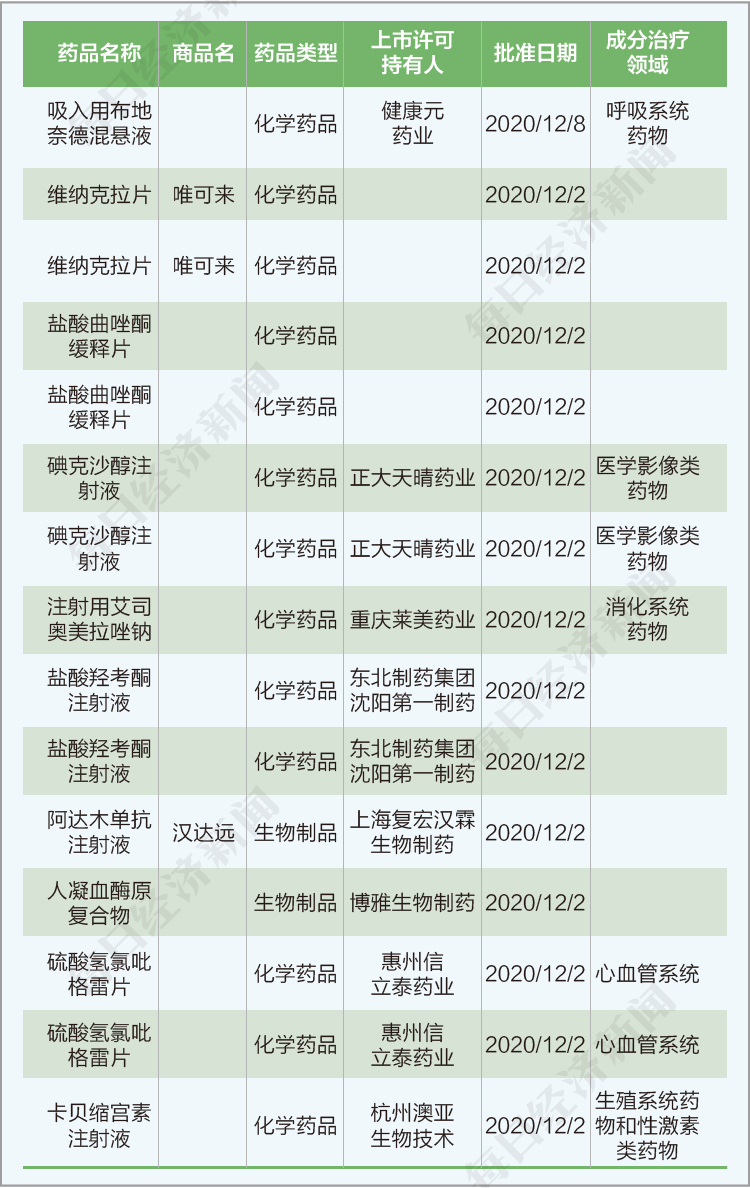
2、本阶段申报的项目中,化药仿制药100项,化药新药/原研药111项,生物制品新药/原研药62项,化药改良型新药6项,非原研/类似药生物制品26项,生物制品改良型新药3项,生物制品类似药1项,暂时不明15项。
按成分治疗领域排名,前五位是抗肿瘤药物(66项),抗感染药物(56项),免疫系统药物(53项),神经系统药物(40项)和心血管系统药物(35项)。

本阶段无药物纳入优先审评审批品种。
本阶段有16个创新药品种开展临床试验。
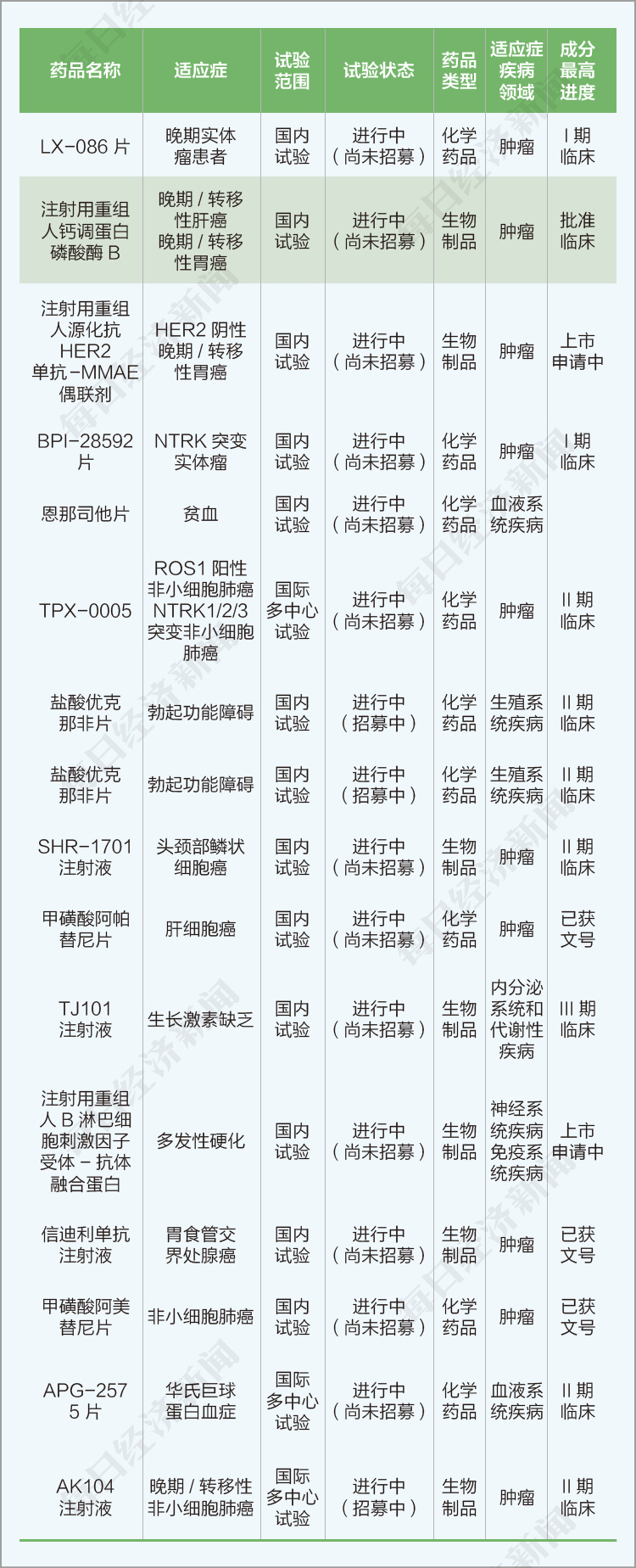
3、本期共有一类注册新药临床申请15个(不含补充申请)。
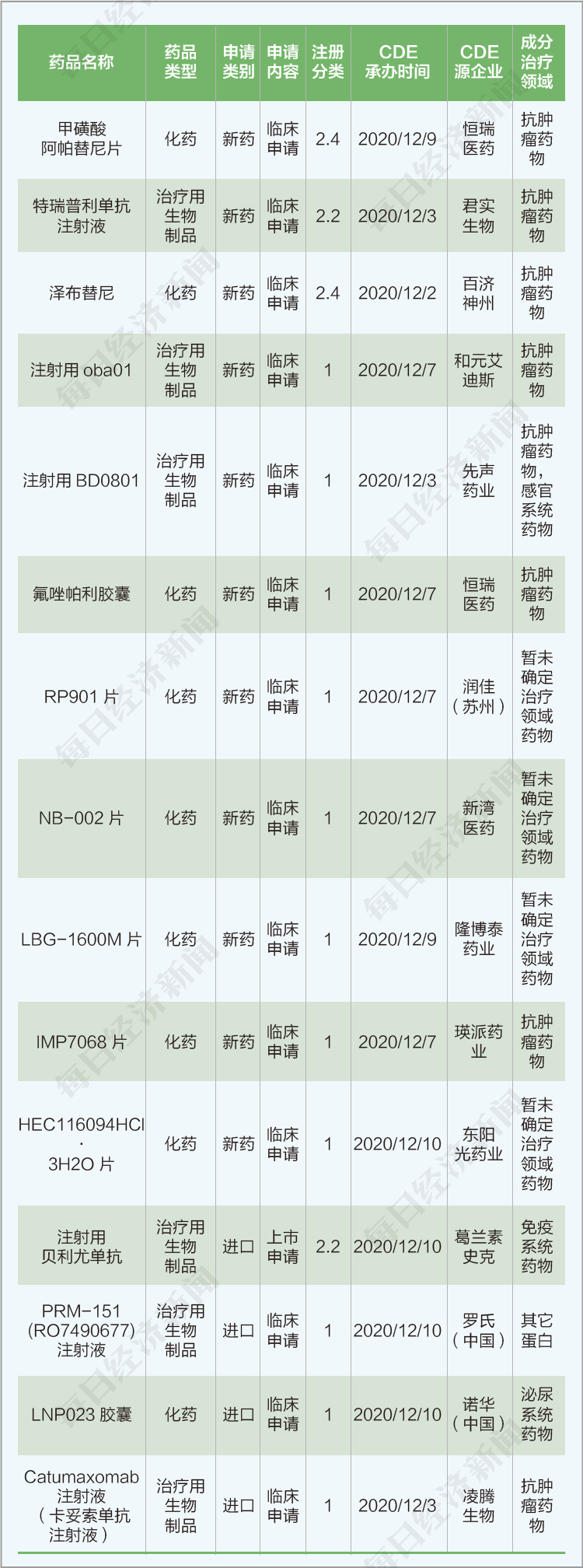
“每经数说丨新药研发”由每日经济新闻编制,每半月发布一次。为避免我们资料收集过程中出现遗漏,请创新药研发企业及时将创新药研发进展通报给我们,以便我们及时计入指数并计算权重。
联络邮箱:jinzhe@nbd.com.cn
封面图片来源:摄图网

1本文为《每日经济新闻》原创作品。
2 未经《每日经济新闻》授权,不得以任何方式加以使用,包括但不限于转载、摘编、复制或建立镜像等,违者必究。
