
和小杨一样,廖玲也是做资质代办业务的。她表示,疫情期间,很多地方的医疗器械备案放宽了审批资质,不管是卖口罩还是卖二类医疗器械等其他产品,都可以很快办理。以前二类医疗器械经营许可属于行政审批事项,平时办理有诸多要求,比如场地、人员等,但是在疫情下,对这类审批放宽了。
每经记者|欧阳凯 叶晓丹 每经编辑|张海妮

图片来源:摄图网
“想把口罩、额温枪等医疗器械卖出国?第一,注册一个公司;第二,办个二类医疗器械经营备案;第三,办理进出口经营权,找我,一步到位。”这是3月13日小杨发在自己微信朋友圈的一条动态,她最近一个多月的朋友圈清一色都是关于口罩资质代办事项。
小杨是深圳一家商事服务公司的咨询顾问,专门为中小企业提供注册/变更、财税审批、政府补贴等服务。2月初以来,因咨询代办口罩资质事项的客户越来越多,她们公司顺势做起了口罩资质代办生意,提供从生产、销售到出口等资质代办的一条龙服务。
疫情之下,口罩需求井喷,许多转产口罩的企业纷纷涌入,这其中,资质申请就是一个门槛。生产及销售口罩,医疗器械经营(生产)许可证+产品注册书、二类医疗器械备案凭证是必备的资质;出口口罩,需要进出口经营权备案及机构认证,一来一回,一些人嗅到了商机,借此做起了代办业务。
“上个月咨询办生产许可、经营备案的比较多,两天之内就有上百个人加我微信,咨询我,后来因为政府收紧了应急备案,现在慢慢少了,不是不能办,只是周期延长了;这个月是咨询口罩出口相关资质办理的比较多。”3月16日,小杨向《每日经济新闻》记者说道。
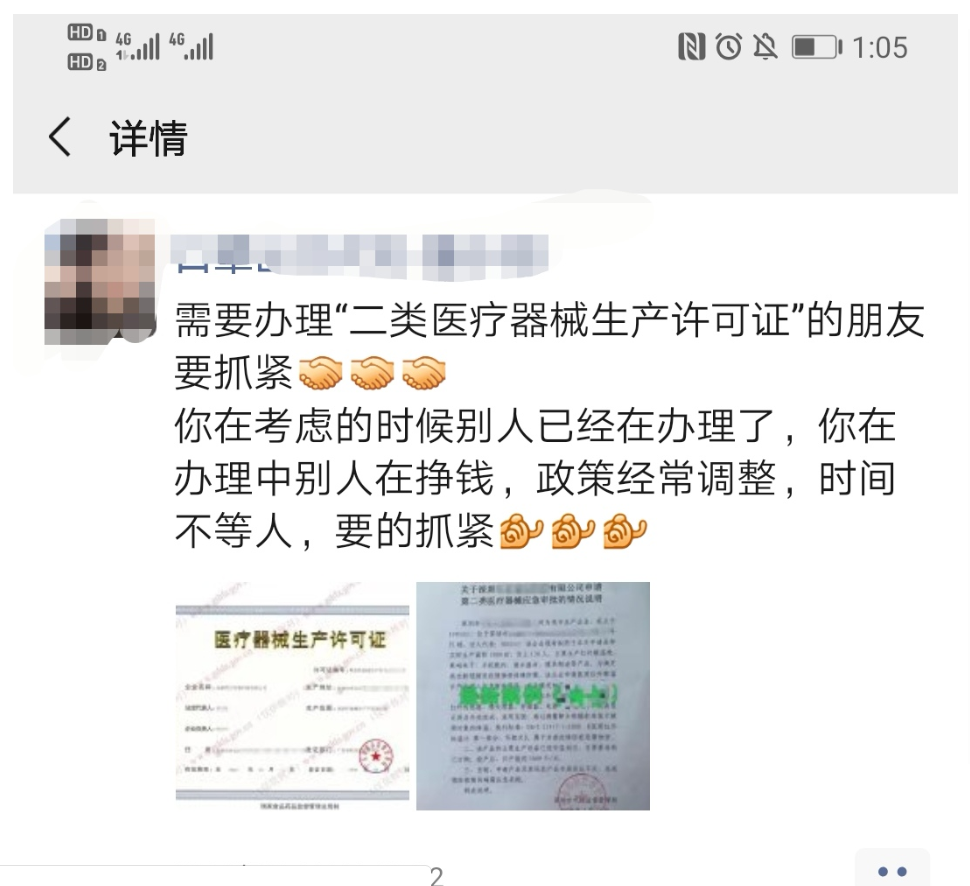
小杨微信朋友圈截图
“有没有留意2月以来有很多涉及口罩的新闻,提到被抓的很多,为什么被抓?要么没货,给钱了不发货,属于诈骗;要么没资质,口罩属于二类医疗器械资质,医用口罩是需要二类医疗器械备案”。谈及口罩相关资质的重要性,小杨告诉记者,很多人因没有这个资质,所以被抓,一般是以非法经营罪定案。
根据相关规定,医疗器械经营许可管理分为三类:经营一类医疗器械无需许可和备案;经营二类医疗器械需备案办理;三类医疗器械许可证需要相关部门审核通过才可办理。
此次疫情中的医用口罩属于国家二类医疗器械,具有各种含有灭菌、抑菌和抗病毒的成分,预期用于抗菌抗病毒的医用口罩属于第三类医疗器械。
和小杨一样,廖玲也是做资质代办业务的。她表示,疫情期间,很多地方的医疗器械备案放宽了审批资质,不管是卖口罩还是卖二类医疗器械等其他产品,都可以很快办理。以前二类医疗器械经营许可属于行政审批事项,平时办理有诸多要求,比如场地、人员等,但是在疫情下,对这类审批放宽了。
《每日经济新闻》记者注意到,早在1月24日,广东省药品监督管理局发布《关于重大突发公共卫生事件一级响应期间对医用口罩等防控急需用器械实施特殊管理的通知》,鼓励各地市场监管部门协助企业准备申请材料,开通绿色通道,帮助相关符合质量标准的企业实现转产,扩大产能。
一周之后,广东省药品监督管理局再度发布《广东省防控新型冠状病毒感染的肺炎疫情所需药品医疗器械行政许可应急审批程序》的通知,对供应紧缺的口罩防护服等物资,纳入应急审批,采取无纸化网上即时受理、先审批后审核、指定专人全程跟进等方式及时保障应急所需。
“在疫情比较紧张的时候,政府开通了绿色通道,设立了备案制度,深圳的领导到企业来调研,多次派专家、处长、科长等到工厂指导我们口罩线的建设,包括环境、产品质量管理等方面。”比亚迪品质处总经理赵俭平告诉记者,在第一批样品顺利通过检测之后,比亚迪拿到了深圳二级医疗器械的应急备案资质。
安吉尔相关负责人告诉记者,公司在2月12日决定生产口罩,查阅了不少生产口罩的资料,并和深圳市的相关卫生部门、市场监管部门都做了沟通,现在生产的KN95口罩已通过了国家最新GB2626-2019标准的各项指标检测,并向深圳市的市场监管部门备案,已具备了正常生产经营的资质和能力。

一次性医用口罩。图片来源:每经记者 张明双 摄
记者调查了解到,在口罩相关资质的代办中,二类生产许可证+产品注册证书(生产)报价在15万~20万元,二类医疗器械备案(销售)报价在1500~3000元,进出口经营权备案(出口)报价在2000~3000元,因口罩需求的增多直接拉动了资质代办服务的接单数量。
3月初,广东省市场监管局局长麦教猛在新闻发布会上介绍,应急备案新增医用口罩生产企业230家,相比省一级响应前的26家增长785%;新增普通口罩生产企业96家。截至3月2日,医用口罩和普通口罩产量合计达2080.89万个/天,比一级响应前增长665%。
但应急备案的热度只维持了一个月,广东省药品监督管理局办公室就下发通知,根据当前疫情防控形势,决定从3月1日起,各市停止疫情防控所需第二类医疗器械应急备案工作。通知还指出,申请应急审批的,应提供所在市联防联控物资保障部门(工信部门)或市场监督管理部门按照模板出具的书面说明。
小杨说,应急备案下只需几个工作日,自己一个人光上月就接了十几单,但3月以来深圳基本已经停批了,按照省里的要求,现在若比较急,只能走应急审批,时间要1个半月,申请口罩生产许可证(含应急审批)+产品注册书的代理费是15万元,包含检测报告费用。
在廖玲看来,申请口罩生产许可证的周期往常是要6至8个月,应急审批虽缩短了时间,但只限疫情期有效,等国家解除疫情了就没有用了,届时要再申请正式的生产许可证。广东、江苏等地的应急备案已转为应急审批,办理周期延长了,对企业的要求也在提高,如相关企业希望申报,还要看企业内部是否合规。
根据廖玲现在的服务方案,办理条件中除了要求客户有与生产的医疗器械相适应的生产场地、环境条件、生产设备,以及专业技术人员、专职检验人员外,还要求企业负责人具备医疗器械相关专业大专以上学历或者中级以上专业技术职称,同时应当具备具有3年以上医疗器械经营质量管理工作经历等。
对此,深圳医协发文指出,随着各地防疫等级的调整,应急产品生产准入的政策也在调整中。目前,广东的口罩生产许可已经收回省局,其相应的审评审批时限较之前有所增加。尚未取得相关生产资质的企业需要对此留意。同时,随着口罩产能持续增长,预计未来国内市场上口罩的供需将逐步稳定,未来随着疫情的好转,口罩的需求也将会逐步回归正常。
《每日经济新闻》记者注意到,目前在国内,疫情受到遏制的趋势已经十分明确,口罩等防护用品供应问题也逐渐得到缓解。但疫情目前在海外蔓延,海外对于口罩等的需求暴增,西班牙、塞尔维亚等部分国家希望中国能够伸出援助之手,一些企业也将目光放到全球口罩紧缺国家的市场。
据记者了解,如果国内企业想出口口罩,需提交提单、箱单、发票、办理进出口经营权,还要同第三方检测认证服务机构合作,由其将企业产品送检查、准备申报材料,将申报材料递交到认证机构。只有通过认证后才可在海外国家出售,其中最受欢迎的当属欧盟的CE认证与美国的FDA认证。
“从上周开始,我们收到了上百家企业关于疫情物资出口的问询,90%以上的问询是关于口罩和消毒剂产品。”杭州瑞欧科技有限公司消费品事业部技术负责人张沫告诉记者,要进行口罩的出口,除了本身口罩在国内完成生产许可、医疗器械注册外,还要有符合产品情况的出口资质。
具体是什么出口资质?张沫解释称,例如医用口罩的出口公司需要在营业执照的经营范围内涵盖二类医疗器械,出口的口罩需要按照对方进口国的要求完成认证(包括检测报告、资质证书等),最后在海关通关时,按照海关的要求准备好提货单等材料,准备齐全的话,一般可以顺利完成产品出口。
小杨说,公司会和第三方检测机构合作,为客户提供认证服务,目前欧盟CE认证(医用口罩)报价15000元,需提交口罩规格名称,3张口罩样品图片,填写申请表格;欧盟CE认证(普通口罩)报价7000元,需营业执照扫描件,样品,办理周期在10个工作日左右。
张沫进一步强调,属于个人防护用品的口罩(国内的KN系列)和医用口罩(包括一次性医用口罩、医用外科口罩、医用防护口罩)的CE认证要求是不同的,非无菌口罩和无菌口罩的CE认证要求也是不同的。
“以个人防护类口罩为例,目前国内认证需求量较大,在检测报告齐全的情况下,国内认证机构一般需要2~3周的时间(有些大型的国际认证机构需要等待1~1.5个月),价格也上涨到了2万~3万元,而在平时,做一份个人防护用品的CE认证费用在1万左右。”张沫说道。
此外,张沫表示,无菌口罩的CE认证难度很大:一方面,欧盟实行了新版医疗器械法规(MDR),材料要求比之前更高;另一方面,无菌口罩的厂家需要完成ISO13485体系认证,所以目前选择去开展无菌医用口罩CE认证的国内企业较少。

图片来源:摄图网
至于美国FDA认证,张沫告诉记者,出口医用口罩的企业需要按照美国510k申请流程获得FDA的510k批准。而个人防护口罩(如N95)需要获得NIOSH(美国国家职业安全卫生研究所)认证,企业需寄送样品至NIOSH实验室实施测试,同时提交技术性资料,在文件审核和产品测试都通过以后,NIOSH会核发认证。
张沫坦言,目前国内中小认证机构并不太愿意承接美国的口罩认证服务:一方面,相关流程时间更长。根据企业的产品资料齐全情况,时间从2个月到10个月不等;另一方面,结果也存在较大不确定性。市面上的FDA医用口罩的认证服务报价在8万~10万元,甚至更高。
谈到美国FDA认证,小杨也向记者坦承,其确实比欧盟CE认证更加苛刻,审批流程复杂,审核周期较长,恐怕做下来也要一年左右,而且费用较高,公司报价在30万元以上,一般不建议客户做。
对于未来是否会将口罩出口,记者采访了比亚迪、安吉尔等转产口罩的企业,得到的说法均是——先保国内需求,如果海外有需求,也不排除口罩出口的可能。比亚迪总裁办主任李巍向记者透露,现在政府也采购了一部分比亚迪的口罩,捐赠给意大利、韩国等疫情比较严重的国家及地区。
“目前国外疫情(形势)严峻,我们已接到国外客户对口罩的迫切需求,确实口罩出口有特殊的认证要求(如欧盟CE、美国FDA),目前我们正在积极申请各类出口的证书,很快就会有安吉尔的口罩出口到国外。”安吉尔相关负责人则对记者称。
《每日经济新闻》记者注意到,目前新纶科技、阳普医疗、长荣股份、佛慈制药等上市公司相继表示公司或子公司涉及口罩等防护用品出口业务或资质。同时,部分上市公司,如三夫户外、首航高科、搜于特、翰宇药业等表示,正加紧筹备口罩出口业务,还有一些公司目前仍在观望中。
张沫称,根据经验,前期咨询CE认证的企业较多,因为早期的口罩需求主要来自于欧洲国家,而且CE流程周期较短,可以快速实现口罩产品出口欧盟,但随着市面上通过CE认证的产品越来越多,以及上周美国宣布全国进入紧急状态后,美国的口罩需求量快速增加,关注美国口罩出口认证的企业也变多了。
不过,3月22日,12360海关热线更新一条最新消息称欧美紧急放宽口罩防控物资准入要求。
欧盟会员会在欧洲官方杂志(Official Journal of the EuropeanUnion)发布了疫情期间针对医疗器械和个人防护用品(PPE)的符合性评价和市场监督程序的建议。值得注意的是,该建议采取紧急措施的内容显示,需要公告机构认证的产品在完成合规性评估程序之前(即取得CE标志之前)可以先出口,但是要确保认证工作会继续完成。采购主体仅限欧盟成员国官方或授权机构采购的防护产品可以没有CE标志,但是只能给医护人员使用,不能在当地市场上销售。而在后续监管中,欧盟成员国的相关市场监督机构会重点抽查这些不带CE标志的产品。

而美国健康与社会服务部(HHS)宣布有必要在新冠肺炎疫情暴发期间紧急使用个人呼吸防护设备、体外检测试剂盒等医疗物资。制造商和战略储备机构可以向美国食品药品管理局(FDA)提出要求,以将其产品添加到紧急使用授权中。

相关链接:

1本文为《每日经济新闻》原创作品。
2 未经《每日经济新闻》授权,不得以任何方式加以使用,包括但不限于转载、摘编、复制或建立镜像等,违者必究。
