每经记者 许立波 每经编辑 陈俊杰
自去年6月18日在港交所敲钟后,科济药业-B(02171,HK)近日交出了上市以来的首份年度业绩报告。
公司官网显示,科济药业是一家在中国及美国开展业务的生物制药公司,主要专注于治疗血液瘤和实体瘤的创新CAR-T 细胞疗法。作为一家创新型生物制药公司,截至目前,科济药业并无产品获批准进行商业销售,也未有产品销售的收益。
2021年全年,科济药业共实现净亏损人民币47.44亿元,较上一年度扩大36.8亿元。其中,发行予投资者的金融工具的公平值亏损为41.56亿元。
从支出端看,因用于支持临床试验的员工人数、员工成本、测试及生产开支增加,公司研发开支由上一年度的2.82亿元增长到5.02亿元;因首次公开发售相关的上市开支及员工人数及员工成本增加,公司行政开支由上一年度的7689.3万元增长到1.26亿元。
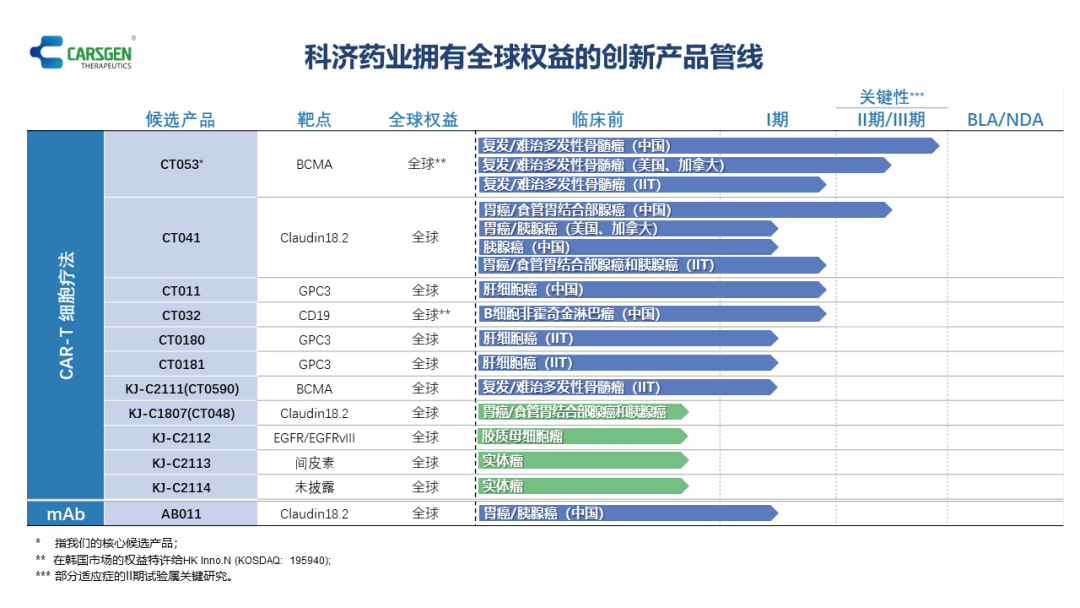
科济药业主要研发管线 图片来源:公司官网
目前,科济药业已建立逾10个创新候选产品管线,研发进展较快的有CT053、CT041等产品。
其中,CT053是一种针对BCMA的自体CAR-T细胞核心候选产品,被开发用于治疗复发/难治多发性骨髓瘤(R/R MM)。在该产品上,科济药业已完成在中国进行的关键II期试验(LUMMICAR STUDY 1)的患者入组,并计划于2022年上半年向国家药监局提交上市申请以及 2023年向FDA提交上市申请。此外,科济药业亦计划进行其他临床试验以开发CT053作为多发性骨髓瘤的早线治疗方法。
CT041是一种潜在全球同类首创的、靶向Claudin18.2(CLDN18.2)蛋白的自体CAR-T细胞候选产品,主要治疗胃癌/食管胃结合部腺癌(GC/GEJ)及胰腺癌(PC)。在该产品上,科济药业已在国内开展了研究者发起的试验、一项针对晚期胃癌/食管胃结合部腺癌和胰腺癌的Ib期临床试验、一项针对晚期胃癌/食管胃结合部腺癌的确证性II期临床试验,并计划于2024年上半年向国家药监局提交上市申请以及2024年向FDA提交上市申请。
报告还披露,在产能方面,科济药业已在CAR-T制造的全部阶段建立了端对端的自主制造能力,包括质粒生产、慢病毒载体生产和CAR-T细胞生产。利用在上海徐汇区的生产厂房以及位于上海金山区的商业GMP生产工厂,公司一直能够自主地生产CAR-T细胞以支持中国的临床试验,及自主地生产慢病毒载体以支持全球的临床试验。
科济药业也持续在中国及美国扩张产能,以支持临床试验和随后管线产品的商业化,公司在美国北卡罗来纳州达勒姆市的三角研究园(RTP)区域建设的 CGMP生产工厂(“RTP生产工厂”)已启动运营。RTP生产工厂总建筑面积约为3300平方米,将每年为700名患者提供额外的自体CAR-T细胞产品产能,也将支持公司正在进行的临床研究及于北美和欧洲的早期商业推广。

1本文为《每日经济新闻》原创作品。
2 未经《每日经济新闻》授权,不得以任何方式加以使用,包括但不限于转载、摘编、复制或建立镜像等,违者必究。
