
◎ 瑞典公共卫生局微生物学研究员米拉齐米告诉《每日经济新闻》记者,mRNA技术与CRISPR基因编辑技术的结合可能是未来探索的潜在路径之一。
每经记者|文巧 每经编辑|兰素英
随着mRNA新冠疫苗的成功推广,mRNA(信使核糖核酸)技术获得了前所未有的关注,也收获了资本市场的青睐。
以行业龙头公司Moderna和BioNTech为例,据Companies Market Cap数据,截至2023年12月26日,Moderna的市值从2020年年初的65.8亿美元飙涨至361.8亿美元,BioNTech的市值也从76.8亿美元升至252.5亿美元,涨幅分别超440%和220%,而同期纳指的涨幅约为66%。
今年的诺贝尔生理学或医学奖更是颁给了科学家卡塔琳·卡里科和德鲁·韦斯曼,表彰他们在mRNA研究上的突破性发现,进一步放大了这一技术的价值。有医疗专家如此描述道,mRNA疫苗技术落地是人类文明史上的又一次“盗火”,这预示着其可能会带来生物医药领域的巨变。
有数据表明,2023年-2028年期间,mRNA疫苗和疗法市场规模将以16.8%的复合年均增长率快速增长,预计在2028年达到1018亿美元。
《每日经济新闻》记者注意到,包括阿斯利康、葛兰素史克、默克、礼来、赛诺菲、辉瑞等跨国医药巨头已经在相关产业加大布局投资。亚太地区有超过60%的疫苗制造商亦有意愿改造或建立新设施,尤其是与mRNA技术相关的设施。
当前,科学家们正在积极探索mRNA技术的未来,希望能够改变人类未来治疗和预防多种疾病的方式。mRNA技术又将如何实现这一突破?又还面临着哪些技术难题?带着这些疑问,《每日经济新闻》记者采访到瑞典卡罗林斯卡医学院实验医学系教授、瑞典公共卫生局微生物学研究员阿里·米拉齐米,以及不列颠哥伦比亚大学生物医学工程学院教授安娜·布莱克尼。
人体依靠数百万种微小的蛋白质来维持自身的生命和健康,并利用mRNA来告诉细胞制造哪些蛋白质。在卡里科曾经的设想中,从理论上讲,如果能够设计mRNA,人体内就拥有了一个蛋白质制造工厂,可以制造任何想要的蛋白——抗感染的疫苗或抗体,治疗罕见疾病的酶,或是修复受损组织的生长剂。
随着mRNA新冠疫苗的成功推广,mRNA技术已远不止于疫苗开发,科学家们现在将注意力转向mRNA 技术的未来,布莱克尼和米拉齐米都认为,该技术有潜力改变人类未来治疗和预防多种疾病的方式。
卡罗林斯卡医学院科学家于2022年11月发表在《自然》上的一篇论文写道,与蛋白质药物相比,mRNA的真正附加价值是合成高水平细胞内蛋白质的能力,这使其能够直接靶向一些在临床技术上很难用蛋白质药物治疗的代谢疾病,或将其应用于紧急护理中,以帮助有急性衰弱和危及生命的疾病的患者。
鉴于mRNA几乎可以在全身或局部产生任何蛋白质,目前科学界正在研究广泛的潜在疾病适应症。布莱克尼向记者说道,“mRNA在癌症疫苗、免疫疗法、蛋白质替代、基因编辑等方面的应用上都有巨大的潜力,这些也是该领域目前正在探索的方向。”
mRNA技术的潜在应用领域 图片来源:每经编辑兰素英制图
谈及基因编辑,米拉齐米认为,mRNA技术与CRISPR基因编辑技术的结合可能是未来探索的潜在路径之一。“我一直在探索结合使用CRISPR/Cas9基因编辑技术和mRNA技术,这可能为对抗复杂疾病的未知疗法打开了大门。”
《每日经济新闻》记者查询发现,一项由mRNA编码的CRISPR-Cas9基因编辑技术治疗遗传性淀粉样变性疾病ATTR的试验在2023年年底启动三期试验。在此前的试验中,该疗法在安全性和有效性方面已经取得了令人鼓舞的结果。
上述论文表示,这项试验的结果将支持探索CRISPR-mRNA疗法对涉及中间代谢缺陷和脂蛋白疾病的多种遗传性肝病的潜在扩展,未来可能会应用于其他实体器官,例如心脏、肾脏和中枢神经系统等。
此外,布莱克尼认为,mRNA 技术的另一大潜力在于提高现有疫苗(如流感疫苗)的功效,“如果我们能够像用该技术合成流感疫苗,那么将大大减少生产所需的时间。如此,我们有可能实时监测流感病毒,并在一个冬天开发出3~4种更有效的疫苗株。”
“mRNA平台有很好的临床数据结果,已经很有说服力。这个平台的优势是非常快、非常灵活,你不需要细胞就可以合成(mRNA)。”阿里·米拉齐米告诉《每日经济新闻》记者。“我相信,它对于癌症治疗,以及一些其他的遗传疾病都可以适用。如今,这个平台实际上已经开始针对癌症治疗进行研究,一些研究已经进行到二期和三期试验的步骤。”
“未来,我认为我们很快会开发出针对其他传染病和癌症的mRNA疫苗。”布莱克尼如此说道。
每经记者注意到,Moderna正在开发针对 RSV、HIV、寨卡病毒、Epstein-Barr 病毒等的mRNA疫苗,该公司计划在未来五年内推出多达15种新产品,并将多达50种mRNA药物推进至临床试验阶段。BioNTech也在探索用于结核病、疟疾、艾滋病毒、带状疱疹和流感的疫苗。除此之外,两家公司还致力于将mRNA技术用于癌症治疗。
目前,全球有几十项临床试验与mRNA肿瘤疫苗有关,涉及黑色素瘤、胰腺癌、结直肠癌等。今年2月,Moderna与默沙东的肿瘤新抗原mRNA疫苗mRNA-4157与PD-1抗体联合辅助治疗高危黑色素瘤,获FDA的突破性疗法认证,这是全球首个获此认证的mRNA肿瘤疫苗。
回顾mRNA疫苗的发展历程,安娜·布莱克尼告诉《每日经济新闻》记者,“当我开始研究RNA 疫苗时,业内外对于mRNA疫苗的有效性仍然存在很多怀疑,更不用说自扩增式RNA疫苗了。尽管我认为mRNA技术最终会取得成功,但如果不是新冠疫苗的推动,它可能还需要更长的时间。”
阿里·米拉齐米也在采访中对记者称,“大流行的确加快了mRNA疫苗的推广进程,尽管我相信这种疫苗早已经是试验中的候选疫苗了。”
科学家卡塔琳·卡里科和德鲁·韦斯曼在今年摘得诺贝尔生理学或医学奖桂冠,也充分说明了mRNA技术对人类的价值。
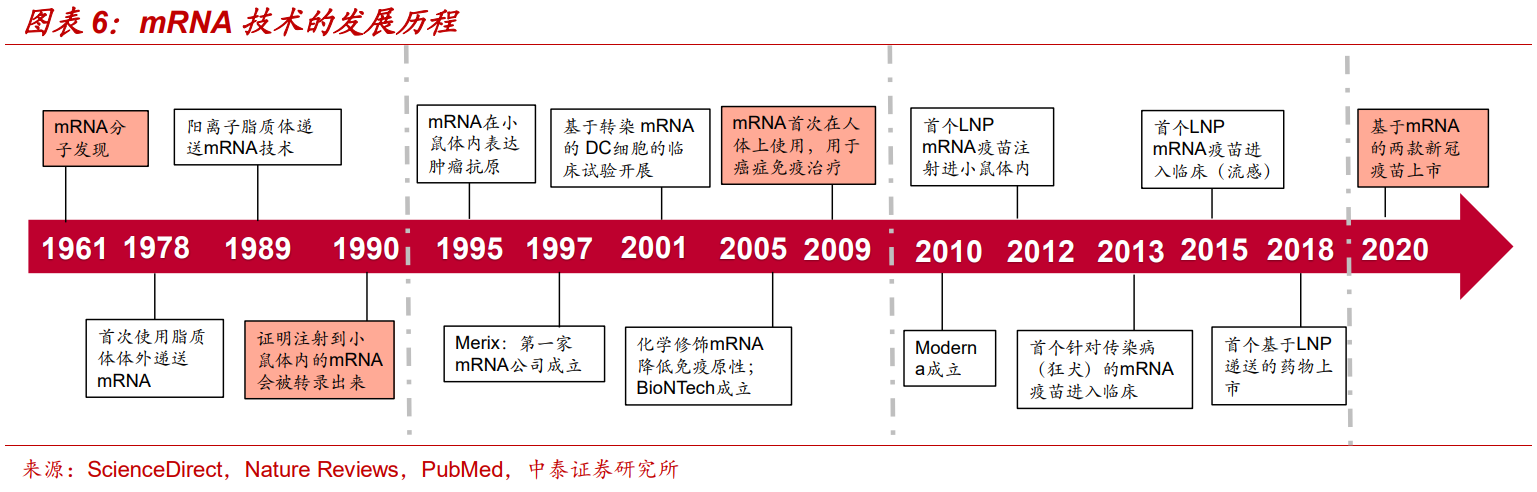
图片来源:中泰证券研究报告
“mRNA新冠疫苗在大流行期间能得以快速推广的原因是开发速度较快(值得注意的是,开发速度与试验速度是不同的)。与传统方法相比,设计和制造mRNA疫苗要简单得多。由于这些疫苗高度安全、有效且率先上市,因此获得了成功。”布莱克尼对每经记者说道。
新冠疫情催生了mRNA疫苗市场的快速增长。根据研究公司 Roots Analysis的数据,2020 年,鉴于新冠大流行带来的迫切需求,专注mRNA 疫苗和疗法开发的公司投资超过52亿美元,远高于2019年的5.96 亿美元。
mRNA疫苗研发企业也在二级市场大放异彩。以该领域的龙头企业Moderna和BioNTech为例,2020年年初迄今,Moderna股价涨幅已经超过385%,BioNTech股价在此期间的涨幅超过215%。
新冠疫情消退之后,市场的目光开始聚焦在更多mRNA疫苗和相关药物疗法上。据中信证券研报测算,mRNA预防性疫苗有望在2025年503亿美元疫苗市场中达到20%渗透率,对应市场规模101亿美元;mRNA肿瘤疫苗有望在2025年达到0.5%渗透率,对应市场规模105亿美元;mRNA蛋白替代疗法有望取代部分蛋白药物市场,预计对应市场规模为66亿美元。

图片来源:中信证券研究报告
国际市场研究和咨询公司Mordor Intelligence的报告数据则透露出该市场更广阔的前景。数据显示,mRNA疫苗和疗法市场规模在2023年将达到468.3亿美元,之后将以16.8%的复合年均增长率快速增长,在2028年预计将达到1018亿美元。报告显示,受研发和投资增加、新产品推出以及慢性病数量增加等因素影响,北美地区当前仍是主要的市场,但亚太地区未来的发展潜力十分强劲。
据上述报告,目前mRNA疫苗和疗法市场的主要玩家包括辉瑞、Moderna、BioNTech、葛兰素史克、第一三共。其他市场参与者包括阿斯利康、默克、礼来、赛诺菲等全球医药巨头,以及CureVac、Arcturus Therapeutics、Translate Bio和Argos Therapeutics等生物科技初创公司。
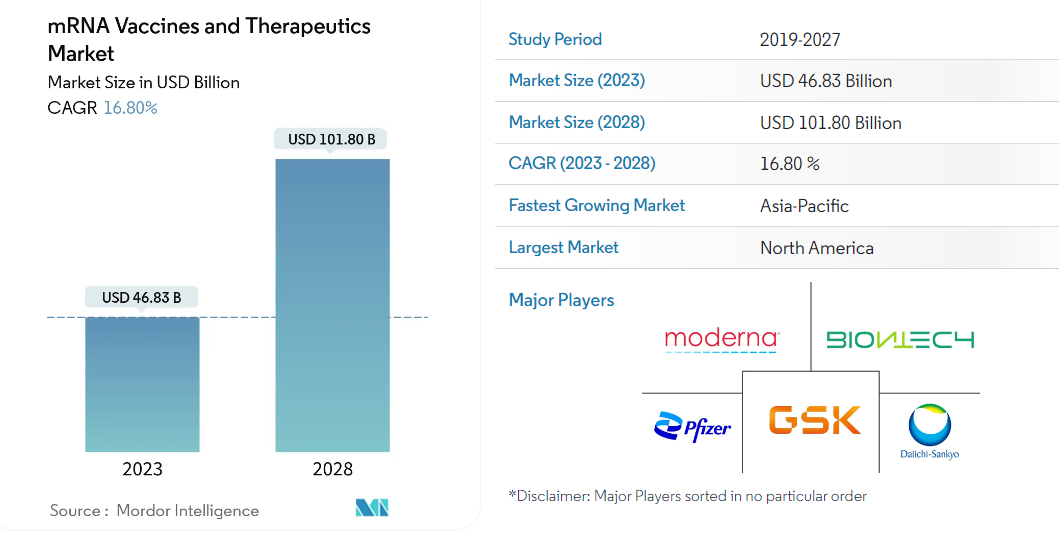
图片来源:Mordor Intelligence网站
自2021年以来,全球医药巨头都在积极实施各种战略以增强自身在mRNA领域的实力。举例来说,2023年4月,Moderna与IBM合作探索下一代技术,包括量子计算和人工智能,以推进和加速mRNA研究和科学;6月,加拿大医药巨头Providence Therapeutics与加拿大健康研究机构宣布合作开发基于mRNA的疫苗和疗法。
在mRNA之外,更大的RNA药物疗法领域也受到了投资界的青睐,包括小干扰RNA(siRNA)、核酸适配体(RNA aptamer)和转运RNA(tRNA)等。
据医药生物技术平台公司药明康德的内容团队不完全统计,2019年~2023年,全球RNA药物领域共发生超过400起融资事件;截至2023年11月,一共发生76起融资事件,其中,有37起融资突破1亿元人民币,破亿融资事件占比接近50%。
据悉,2023年,该领域超过一半(55%,42起)是早期融资事件(A轮及A轮前),总融资金额比2022年提高了24%,达到79亿元,有望超越2021年的融资水平。目前该领域单笔最高融资也来自ReNAgade Therapeutics的超3亿美元A轮融资。
尽管市场前景广阔,但当前mRNA疗法的开发和推广仍然还面临着不小的挑战。布莱克尼对《每日经济新闻》记者表示,“对于mRNA疗法的开发,我预计还将需要更多时间,因为在涉及免疫原性和剂量的问题上仍然存在很大的问题。”
卡罗林斯卡医学院科学家在《自然》上发表的论文中也提到了这一点问题,“mRNA 固有的免疫原性虽然增强了其作为疫苗的功效,但阻碍了其作为治疗剂的使用,因为治疗剂需要更高水平的蛋白质表达。”
具体来讲,通过注射疫苗产生免疫反应只需要最少量的蛋白质(mRNA),因为免疫系统可以通过细胞介导和抗体介导的免疫显著放大抗原信号。但相比之下,通过mRNA疗法来治疗其他疾病则需要高达1000倍的蛋白质水平才能达到治疗阈值。
另一方面,论文提到,治疗剂量高度依赖于给药途径。在许多情况下,mRNA疗法必须要有特定的靶途径、细胞、组织或器官,这意味着靶细胞的摄取效率将非常重要,因为其决定了蛋白质表达的持续时间和水平。除了肝脏(常用的静脉注射靶向器官)之外,如何将mRNA有效递送到实体器官仍然具有挑战性。实现 mRNA 疗法的全部潜力将需要更先进的体内递送系统,特别是对于心脏、肾脏、大脑和肺等实体器官。
这就提出了有关临床靶点设计的难题。布莱克尼表示,“当前开发mRNA技术最主要的挑战还包括设计RNA(的靶点)和递送系统,以按所需方式激活或不激活免疫系统,基本上每种疫苗和疗法的情况都不同。”
据《麻省理工学院科技评论》的一篇文章,癌症疫苗的制造比较困难,部分原因是,当人体细胞形成肿瘤时,通常没有像新冠病毒上的刺突蛋白那样明确的蛋白质靶标。
在布莱克尼看来,对于艾滋病毒来说,找到良好靶标也存在难度。“科学家还从未发现针对艾滋病毒能够诱导有效免疫反应的蛋白质(靶标)。”
“在技术方面,RNA和相关制剂的质量控制仍然存在挑战。我们还需要有更多的时间才能够更好地理解该技术的系统和结构功能关系。”布莱克尼告诉《每日经济新闻》记者。“安全性也是临床试验不可或缺的一个方面。实际上,mRNA 疫苗的首次临床试验已于十多年前开始,因此我们确实拥有长期的安全性数据。”
“总的来说,我认为mRNA技术的好处在于它的开发速度相对较快且制造成本低廉,我希望全球范围内能更公平地获得这些药物。”她总结道。
封面图片来源:视觉中国-VCG11385119793

1本文为《每日经济新闻》原创作品。
2 未经《每日经济新闻》授权,不得以任何方式加以使用,包括但不限于转载、摘编、复制或建立镜像等,违者必究。
