赴港上市近一年,复宏汉霖-B(02696,HK)迎来了第二款商业化产品。
公司汉曲优®(注射用曲妥珠单抗,欧盟商品名:Zercepac®)于今年7月和8月相继获得欧盟委员会及国家药品监督管理局批准上市,成为首个中欧双批的国产单抗生物类似药,可用于HER2阳性早期乳腺癌、转移性乳腺癌和转移性胃癌的治疗。
8月30日,在上海生物医药产业国际化发展论坛暨首个国产曲妥珠单抗中欧上市新闻发布会上,复宏汉霖联合创始人、首席执行官刘世高在接受包括每日经济新闻在内的媒体采访时表示,“这次(汉曲优®)进欧盟,我们打的是‘世界杯’,而不是一个(局限在)国内或者亚洲的比赛。”

复宏汉霖联合创始人、首席执行官刘世高 图片来源:主办方供图
中国籍生物药要打“世界杯”
中国医药企业参与单抗生物类似药“世界杯”比赛,这是头一次。
据艾昆玮咨询业务高级总监李浛君介绍,单抗生物药是近五年来生物药领域增长最快的一个类别。但同时,因为具有研发壁垒高、工艺开发难、生产要求高等诸多特点,单抗药研发周期长、投入高。
据了解,汉曲优项目启动于2010年,自2015年开始开展国际多中心3期临床试验;2018年,复宏汉霖与全球性制药公司Accord签订许可协议,授权后者获得在欧洲地区53个国家、中东及北非地区17个国家和部分独联体国家对汉曲优的独家商业化许可;同时,复宏汉霖还与Cipla、Mabxience等国际一流的生物制药企业达成合作,持续推动产品商业化进程,累计覆盖全球80多个国家和地区。
刘世高此前在接受《每日经济新闻》记者专访时表示,在中欧上市之后,公司也有意推动汉曲优®在美国上市,“HLX02(汉曲优®)的临床数据非常好,跟原研药赫赛汀同样在欧盟获批上市,毫无疑问是具备国际标准的,而且价格更便宜,我们相信这个产品能得到医生和患者的认可,公司也在寻求HLX02在美国上市,目前正在积极地跟FDA沟通,看是否需要补充提交相关材料。”
在复宏汉霖总裁张文杰看来,汉曲优®在欧洲上市,对于公司和国内生物制药行业而言是里程碑事件,“这只是第一步,接下来我们会进一步在美国以及其他创新产品全球市场进行开拓,包括发达市场和新兴市场,这是中国生物制药早晚要走的一条路径。”
竞技场竞争激烈
汉曲优®的原研药是罗氏的赫赛汀,赫赛汀于1998年在美国上市,上市二十余年,赫赛汀一直是HER2阳性乳腺癌治疗的“金标准”药物。
近年来,专利期的到来对赫赛汀的销售额造成一定冲击。据了解,赫赛汀在欧盟的专利已于2014年7月到期,美国专利也于2019年6月到期。罗氏2019财报显示,报告期内受欧洲、日本和美国生物类似药竞争的影响,赫赛汀的销量下降了12%;罗氏2020上半年财报显示,以恒定汇率计算,赫赛汀营收22亿瑞郎,同比下降28%,其中美国市场下降最严重,降幅达42%,其次是日本,降幅达37%。
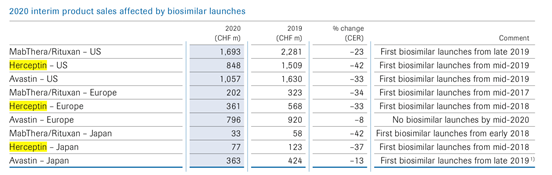
2020上半年赫赛汀销售额受生物类似药影响情况
这也意味着,尽管是首个中欧双批的国产单抗生物类似药,但放眼到国际市场,汉曲优®要想分走“蛋糕”,仍然面对诸多对手。在欧洲市场方面,已上市的曲妥珠单抗除了赫赛汀,还包括Celltrion的Herzuma®,Samsung Bioepis的Ontruzant®等。据IQVIA MIDASTM数据估计,2019年原研曲妥珠单抗及其生物类似药在欧洲地区的销售额为13.68亿美金。
美国市场方面,已有5款赫赛汀的生物类似药获得FDA的获批上市,分别是Mylan和Biocon开发的Ogivri®,Celltrion的Herzuma®,辉瑞的Trazimera®、安进和艾尔建的Kanjinti®以及默沙东的Ontruzant®。
国内市场方面,赫赛汀于2017年进入国家医保目录,价格定为7600元/440mg,2019年,新版国家医保目录调整,赫赛汀价格降至5500元/440mg。复宏汉霖总裁张文杰介绍称,汉曲优的定价是1688元/支,每支的规格是150mg。“因为跟原研药规格不同,很难在定价上作直接对比,对于不同规格和不同剂量,国家发改委有规定好的转换公式。”
走“城乡并进”的商业化道路
尽管受制于规格不同,很难与原研药在价格上进行直接对比,但在上海市生物医药行业协会会长傅大煦看来,生物类似药真正要成为患者“用得起”的药物,可能还要一个过程。“因为现在用的装备、分离介质、反应袋、培养基全是进口,真正做让患者‘用得起’,为患者健康服务的药物,行业同仁需继续努力,继续奋进。我相信抗体药物的前景,还是十分广阔的。”
刘世高也曾向《每日经济新闻》记者透露,公司生产涉及的相关材料在寻求国产代替进口,“其实就是为了降本增效,我们在保证质量一致的前提下,用国产代替进口,有利于降低成本,首先进口税这一块就可以大大降低。”
在商业化方面,张文杰将汉曲优的商业策略概括为“城乡并进”,“我们会多方挖掘市场潜力,核心市场和广阔市场都会给予同样重视,因为核心市场是未来新产品上市的制高点,但我们的主旨是‘不让一个HER2+患者落下’,所以对于广阔市场,尤其是那些未被最佳治疗的患者,我们会不遗余力给他们提供最好的治疗。”
张文杰进一步表示,“政府对生物类似药给了很多支持,药品一上市就自动属于国家医保,但每个省的医保落地需要时间,所以我们接下来4个月的工作重点就是全力以赴做准入,同时我们也已经与商业保险展开合作,通过额外的商业保险给予病人在医保之外更好的保险服务。”
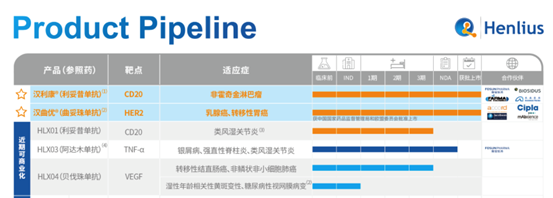
复宏汉霖已上市及近期可商业化的产品
产品管线方面,公开资料显示,公司的贝伐珠单抗已于本月完成治疗转移性结直肠癌的3期临床研究,且已达到预设的主要及次要研究终点;阿达木单抗目前已递交NDA上市申请;利妥昔单抗(汉利康®)已经获批原研药在中国获批的全部适应症,同时公司对汉利康®采取差异化的开发策略,同步开展原研药在国内尚未获批的类风湿关节炎适应症的临床研究,目前该项3期临床试验已经完成患者入组。此外,复宏汉霖还拥有二十余个临床在研和临床前的产品。
刘世高表示,未来公司在创新药研发方面将重视与国际药厂的合作,“这也是我们降低风险的方式之一,通过跟国际药厂或者是有相同理念的生物技术公司合作,可以共担风险,共享资源,以同样的投资去做更多的品种,也有更高的成功上市机会。”
封面图片来源:摄图网












